In this article, we will share MP Board Class 12th Chemistry Solutions Chapter 8 d एवं f-ब्लॉक के तत्त्व Pdf, These solutions are solved subject experts from the latest edition books.
MP Board Class 12th Chemistry Solutions Chapter 8 d एवं f-ब्लॉक के तत्त्व
d एवं f-ब्लॉक के तत्त्व NCERT पाठ्यनिहित प्रश्नोत्तर
प्रश्न 1.
आद्य अवस्था में सिल्वर परमाणु में पूर्ण भरे d-कक्षक (4d10) होते हैं। इसे आप कैसे कह सकते हैं कि यह संक्रमण तत्व है?
उत्तर
सिल्वर +2 ऑक्सीकरण अवस्था रखता है। 4d-उपकक्ष में नौ इलेक्ट्रॉन होते हैं, जैसे 4dकक्षकों का एक कक्ष आंशिक भरा होता है। अतः इसे संक्रमण तत्व नहीं मान सकते।
प्रश्न 2.
श्रेणी Sc(Z = 21) से Zn(Z = 30) में, Zn की परमाणुकरण की एन्थैल्पी कम होती है, 126 kJmol-1 क्यों?
उत्तर
जिंक में 3d-इलेक्ट्रॉन धात्विक बन्ध में भाग नहीं लेते क्योंकि d10 विन्यास होता है। दुर्बल धात्विक बंध के कारण जिंक की परमाणुकरण की एन्थैल्पी निम्न होती है।
प्रश्न 3.
संक्रमण धातुओं की 3d श्रेणी में किसकी अधिकतम संख्या में ऑक्सीकरण अवस्था होती है एवं क्यों ?
उत्तर
Mn(Z = 25) अधिक संख्या में ऑक्सीकरण अवस्थायें रखते हैं, क्योंकि इसमें अधिकतम संख्या में अयुग्मित इलेक्ट्रॉन होते हैं। अत: यह +2 से +7 तक ऑक्सीकरण अवस्थायें दर्शाता है।
प्रश्न 4.
E°(M2+/M) का मान कॉपर के लिए धनात्मक (+034V) है। इसका संभावित कारण क्या है ? (संकेत : इसकी उच्च ΔaH⊖ एवं निम्न ΔhydH⊖ मानने पर) –
उत्तर
किसी धातु की E° (M2+/M) पूर्ण परमाणुकरण की एन्थैल्पी, आयनन एन्थैल्पी एवं जलयोजन एन्थैल्पी पर निर्भर होती है। कॉपर की उच्च परमाणुकरण एन्थैल्पी एवं निम्न आयनन एन्थैल्पी होती है। अतः E° (Cu2+ /Cu) धनात्मक है।
प्रशन 5.
संक्रमण तत्वों की प्रथम श्रेणी में (प्रथम एवं द्वितीय) आयनन एन्थैल्पियों में अनियमित क्रमिकता को किस प्रकार देखते हो? ।
उत्तर
आयनन एन्थैल्पी में अनियमित क्रम (प्रथम एवं द्वितीय) का कारण मुख्यतः विभिन्न 3dविन्यासों के भिन्न स्थायित्व की मात्रा के कारण होता है। d0, d5 एवं d10 विन्यास अतिरिक्त स्थायित्व रखता है एवं ऐसे प्रकरणों में आयनन एन्थैल्पी के मान सामान्यत: उच्च होते हैं। उदाहरण, Cr के प्रथम आयनन एन्थैल्पी के नाम निम्न होते हैं, क्योंकि 4s- कक्षक से इलेक्ट्रॉन को निकाला जा सकता है, किन्तु द्वितीय आयनन एन्थैल्पी अति उच्च होती है, अत: Cr+ में स्थायी d5 विन्यास होता है। Zn की प्रथम आयनन एन्थैल्पी अति उच्च होती है, क्योंकि स्थायी विन्यास 3d10,4s2 से इलेक्ट्रॉन हटाया जाता है।
प्रश्न 6.
धातु अपने उच्चतम ऑक्सीकरण अवस्था में केवल ऑक्साइड अथवा फ्लोराइड में रहते हैं, क्यों?
उत्तर
क्योंकि ऑक्सीजन एवं फ्लुओरीन का आकार छोटा एवं ऋण-विद्युतता उच्च होती है, इस प्रकार ये सरलता से धातु को उसकी उच्च ऑक्सीकरण अवस्था में ऑक्सीकृत करता है।
प्रश्न 7.
Cr2+ अथवा Fe2+ में से कौन-सा प्रबल अपचायक अभिकर्मक है एवं क्यों ?
उत्तर
Fe2+ से Cr2+ प्रबल अपचायक अभिकर्मक है। इसका कारण है कि Cr2+ का विन्यास d4 ‘से d3 एवं d3 विन्यास में परिवर्तित होता है, जो स्थायी t32(g)(138) अर्द्धपूर्ण t2) स्तर है।
प्रश्न 8.
M2+(aq) आयन (Z = 27) के लिए ‘चक्रण खेल’ चुम्बकीय आघूर्ण की गणना कीजिए।
उत्तर
M2+(aq) आयन (Z = 27) का इलेक्ट्रॉनिक विन्यास है :
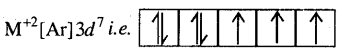
इस प्रकार तीन अयुग्मित इलेक्ट्रॉन हैं। ‘चक्रण केवल’ चुम्बकीय आघूर्ण
![]()
प्रश्न 9.
Cu+ आयन जलीय विलयनों में क्यों स्थायी नहीं हैं, समझाइये?
उत्तर
Cu+(aq) जलीय विलयन में स्थायी नहीं है, क्योंकि इसकी Cu+(aq) की तुलना में निम्न ऋणात्मक जलयोजन एन्थैल्पी है।
प्रश्न 10.
लैन्थेनॉइड संकुचन की तुलना में तत्वों से तत्वों में एक्टीनॉइड संकुचन अधिक है, क्यों ?
उत्तर
लैन्थेनॉयड के 4f इलेक्ट्रॉनों की तुलना में एक्टीनॉयड्स में 5f इलेक्ट्रॉनों का कमजोर परिरक्षण प्रभाव के कारण होता है।
d एवं f-ब्लॉक के तत्त्व NCERT पाठ्य-पुस्तक प्रश्नोत्तर
प्रश्न 1.
इलेक्ट्रॉनिक विन्यास लिखिए –
(i) Cr3+
(ii) Cu+
(i) CO2+
(iv) Mn2+
(v) Pm3+
(vi) Ce4+
(vii) Lu2+
(viii) Th4+
उत्तर
(i) Cr+3 : [Ar]3d3
(ii) Cu+1 : [Ar]3d10
(iii) CO+2 : [Ar]3d7
(iv) Mn+2 : [Ar]3d5
(v) Pm+3 : [Xe]4f4
(vi) Ce+4 : [Xe]54 .
(vii) Lu+2 : [Xe]4 f145d1
(vii) Th+4: [Rn].
प्रश्न 2.
+3 अवस्था में Mn+2 यौगिक Fe+2 से ऑक्सीकरण में अधिक स्थायी है, क्यों?
उत्तर
Mn+2 का स्थायी इलेक्ट्रॉनिक विन्यास [Ar]4s0,3d5 होता हैं एवं यह सरलता से Mn+3 में परिवर्तित नहीं होता, Fe+2[Ar] 4s0,3d6 ऑक्सीकरण पर Fe+3[Ar] 4s0,3d5 बनाता है जो अधिक स्थायी विन्यास है।
प्रश्न 3.
परमाणु क्रमांक में वृद्धि से संक्रमण तत्वों के प्रथम श्रेणी के पहले आधे की +2 अवस्था अधिक एवं अधिक स्थायी होती हैं, विस्तृत विवेचना कीजिए।
उत्तर
स्कैण्डियम (जो +3 ऑक्सीकरण अवस्था दर्शाता है) को छोड़कर, प्रथम श्रेणी के सभी संक्रमण तत्व +2 ऑक्सीकरण अवस्था दर्शाते हैं । यह 4s के दो इलेक्ट्रॉनों के त्यागने के कारण होता है। प्रथम चरण में, जब हम Ti+2 से Mn+2 की तरफ चलते हैं, तो इलेक्ट्रॉनिक विन्यास 3d2 से 3d5 में परिवर्तित होता है, जिसका अर्थ है अधिक-से-अधिक d-कक्षकों का अर्द्धपूर्ण भरना है, जो +2 अवस्था को अधिक स्थायित्व प्रदान करते हैं।
प्रश्न 4.
संक्रमण तत्वों की प्रथम श्रेणी में ऑक्सीकरण अवस्थाओं के स्थायित्व का निर्धारण इलेक्ट्रॉनिक विन्यासों से कितना किया जा सकता है ? अपने उत्तर को उदाहरण सहित समझाइए।
उत्तर
संक्रमण श्रेणी में, ऑक्सीकरण अवस्थायें अर्द्धपूर्ण अथवा पूर्ण भरे हुए d-कक्षक अधिक स्थायी है। उदाहरण के लिए, Fe(Z = 26) का इलेक्ट्रॉनिक विन्यास [Ar]3d64s2 है। यह दर्शाता है कि विभिन्न ऑक्सीकरण अवस्थाओं में Fe(III) अधिक स्थायी है, क्योंकि यह विन्यास [Ar]3d5 रखता है।
प्रश्न 5.
संक्रमण तत्व के स्थायी ऑक्सीकरण अवस्था, आद्य अवस्था में इनके परमाणुओं के d इलेक्ट्रॉन विन्यासों : 3d3,3d5,3d8 एवं 3d4 में से क्या होगी? ।
उत्तर

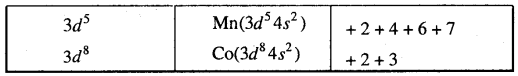
3d4 आद्य अवस्था में कोई d4 विन्यास नहीं होता।
प्रश्न 6.
प्रथम श्रेणी के संक्रमण धातुओं के ऑक्सो धातु ऋणायनों के नाम बताइये, जिसमें धातु की ऑक्सीकरण अवस्था समूह संख्या के बराबर होती है।
उत्तर
CrO2-7 एवं CrO2-4 (समूह संख्या = Cr की ऑक्सीकरण अवस्था = 6) MnO–4 (समूह संख्या = Mn की ऑक्सीकरण अवस्था = 7)
प्रश्न 7.
लैन्थेनॉयड संकुचन क्या है ? लैन्थेनॉयड संकुचन के प्रभाव क्या होंगे?
उत्तर
लैन्थेनाइड संकुचन-लैन्थेनाइडों के परमाणु क्रमांक बढ़ने के साथ-साथ उनके परमाणुओं एवं आयनों के आकार में कमी होती है, इसे लैन्थेनाइड संकुचन कहते हैं।।
कारण-लैन्थेनाइडों में आने वाला नया इलेक्ट्रॉन बाह्यतम कक्ष में न जाकर (n-2)f- उपकोश में प्रवेश करता है, फलतः इलेक्ट्रॉन और नाभिक के मध्य आकर्षण बल में वृद्धि होती है, जिससे परमाणु अथवा आयन संकुचित हो जाता है।
लैन्थेनाइड संकुचन का प्रभाव :
(i) लैन्थेनाइडों के गुणों में परिवर्तन-लैन्थेनाइड संकुचन के कारण इनके रासायनिक गुणों में बहुत कम परिवर्तन होता है। अतः इन्हें शुद्ध अवस्था में प्राप्त करना अत्यन्त कठिन होता है।
(ii) अन्य तत्वों के गुणों पर प्रभाव-लैन्थेनाइड संकुचन का लैन्थेनाइडों से पूर्व आने वाले तथा इनके बाद आने वाले तत्वों के आपेक्षिक गुणों पर बहुत महत्वपूर्ण प्रभाव पड़ता है। उदाहरण के लिए, Ti और Zr के गुणों में भिन्नता होती है, जबकि Zr और Hf गुणों में काफी समानता रखते हैं।
प्रश्न 8.
संक्रमण तत्वों के अभिलक्षण क्या हैं एवं इन्हें संक्रमण तत्व क्यों कहते हैं ? कौन से dब्लॉक तत्वों को संक्रमण तत्व नहीं माना जा सकता?
उत्तर
संक्रमण तत्व वे तत्व हैं जिसके अणुओं में (स्थायी ऑक्सीकरण अवस्था में) आंशिक रूप से पूर्ण d-ऑर्बिटल विद्यमान होते हैं। इन तत्वों को d-ब्लॉक के तत्व भी कहते हैं, ये 5-ब्लॉक तथा p-ब्लॉक के तत्वों के गुणों में संक्रमण प्रदर्शित करते हैं। इसलिए इन्हें संक्रमण तत्व कहा जाता है। Zn, Cd एवं Hg जैसे तत्वों को संक्रमण तत्वों की श्रेणी में नहीं रखा जा सकता क्योंकि इनमें पूर्ण पूरित d-उपकक्षक पाये जाते हैं।
प्रश्न 9.
नॉन-संक्रमण तत्वों से संक्रमण तत्वों के इलेक्ट्रॉनिक विन्यास किस प्रकार भिन्न हैं ?
उत्तर
संक्रमण तत्वों में d-कक्षकों को भरते हैं, जबकि प्रतिनिधि तत्वों में 5-एवं p-कक्षकों को भरते हैं। संक्रमण तत्वों के सामान्य इलेक्ट्रॉनिक विन्यास (n-1)d1-10ns1-2 है, जबकि प्रतिनिधि तत्वों का सामान्य इलेक्ट्रॉनिक विन्यास ns1-2 अथवा ns2np1-6 होता है। प्रतिनिधि तत्वों में केवल अंतिम कक्ष अपूर्ण होता है जबकि संक्रमण तत्वों में उपात्य कक्ष अपूर्ण होता है।
प्रश्न 10.
लैन्थेनॉयड्स कौन-सी विभिन्न ऑक्सीकरण अवस्थायें रखते हैं ?
उत्तर
लैन्थेनॉयड्स का मुख्य ऑक्सीकरण अवस्था + 3 है। इसके अतिरिक्त ये + 2 एवं + 4 ऑक्सीकरण अवस्थायें रखते हैं।
प्रश्न 11.
कारण सहित समझाइए-
(i) संक्रमण धातुओं एवं इनके अनेक यौगिक अनुचुम्बकीय व्यवहार दर्शाते हैं।
(ii) संक्रमण धातुओं के परमाण्वीयकरण की एन्थैल्पी उच्च होती है।
(iii) संक्रमण धातुएँ सामान्यतः रंगीन यौगिक बनाते हैं।
(iv) संक्रमण धातुएँ एवं इसके अनेक यौगिक अच्छे उत्प्रेरक होते हैं।
उत्तर
(i) जब किसी यौगिक को चुम्बकीय क्षेत्र में रखा जाता है तो यौगिक के भीतर का चुम्बकत्व बाहरी चुम्बकीय क्षेत्र से प्रभावित होता है। यदि भीतर का चुम्बकत्व बाहरी चुम्बकीय क्षेत्र का साथ देता है तो उसे अनुचुम्बकीय गुण कहते हैं। यदि यौगिक में अयुग्मित इलेक्ट्रॉन हो तो अनुचुम्बकत्व प्रबल हो जाता है अर्थात् किसी यौगिक के अनुचुम्बकत्व की मात्रा उसमें उपस्थित अयुग्मित इलेक्ट्रॉनों पर निर्भर होती है। संक्रमण तत्वों में अयुग्मित इलेक्ट्रॉन होते हैं, अतः वे अनुचुम्बकीय होते हैं। .
(ii) संक्रमण धातुओं में उच्च प्रभावी न्यूक्लियर आवेश तथा संयोजी इलेक्ट्रॉनों की अधिक संख्या होती है इसलिए ये बहुत मजबूत धात्विक बंध बनाते हैं। परिणामस्वरूप संक्रमण धातुओं के परमाण्विकरण की एन्थैल्पी उच्च होती है।
(iii) संक्रमण धातु आयनों का रंग अपूर्ण रूप से भरे हुए (n-1)d कक्षकों के कारण होता है। संक्रमण धातु आयनों में जिनमें अयुग्मित d-इलेक्ट्रॉन हैं, इस इलेक्ट्रॉन का एक d-कक्षक से दूसरे d-कक्षक में संक्रमण होता है। इस संक्रमण के समय वे दृश्य प्रकाश के कुछ विकिरणों का अवशोषण करते हैं तथा शेष विकिरणों को रंगीन प्रकाश के रूप में उत्सर्जित कर देते हैं। अत: आयन का रंग उसके द्वारा अवशोषित रंग का पूरक (Complementary) होता है। उदाहरणार्थ, [Cu(H2O)6]+2 आयन नीला दिखता है, क्योंकि यह दृश्य प्रकाश के लाल रंग को इलेक्ट्रॉन के उत्तेजना के लिए अवशोषित करता है तथा उसके पूरक (नीले) रंग को उत्सर्जित कर देता है।
कुछ आयनों के रंग –
Cr4+ नीला : Cr3+ बैंगनी
Mn2+ बैंगनी : Mn3+ गुलाबी
Fe2+ हरा : Fe3+ पीला
(iv) संक्रमण तत्व परिवर्ती संयोजकता प्रदर्शित करते हैं, क्योंकि (n-1)d-कक्षक तथा ns-कक्षक के इलेक्ट्रॉनों की ऊर्जा में बहुत अधिक अन्तर नहीं होता है, जिससे d-कक्षक के इलेक्ट्रॉन भी संयोजी इलेक्ट्रॉन का कार्य करते हैं। इन तत्वों में Mn अधिकतम परिवर्ती संयोजकता प्रदर्शित करता है।
प्रश्न 12.
अन्तराकाशी यौगिक क्या है ? संक्रमण धातुओं के ऐसे यौगिक क्यों ज्ञात हैं ?
उत्तर
अधिकांश संक्रमण तत्व उच्च ताप पर अधात्विक तत्वों के परमाणुओं जैसे-H, B,C, Ni, Si आदि के साथ अन्तराकाशी यौगिक बनाते हैं। संक्रमण धातु के क्रिस्टल जालक के अन्तराकाशी रिक्तियों में ये अधात्विक तत्वों के छोटे परमाणु ठीक-ठीक फिट हो जाते हैं। ये अन्तराकाशी यौगिक कहलाते हैं।
प्रश्न 13.
नॉन-संक्रमण धातुओं से संक्रमण धातुओं की परिवर्ती ऑक्सीकरण अवस्थायें भिन्न कैसे होती हैं ? उदाहरण देकर समझाइए।
उत्तर
संक्रमण तत्वों में उत्तरोत्तर ऑक्सीकरण अवस्थाओं में इकाई का अन्तर आता है। उदाहरण के लिए, Mn सभी ऑक्सीकरण अवस्थायें +2 से +7 दर्शाता है। जबकि नॉन-संक्रमण धातुएँ परिवर्ती ऑक्सीकरण अवस्थाएँ रखती हैं, जिनमें दो इकाई का अन्तर होता है, उदाहरण के लिए Pb(II), Pb(IV), Sn(II), Sn(IV).
प्रश्न 14.
आयरन क्रोमाइट अयस्क से पोटैशियम डाइक्रोमेट के बनाने की विधि का वर्णन कीजिए। पोटैशियम डाइक्रोमेट विलयन की pH बढ़ाने पर क्या प्रभाव होगा?
उत्तर
बनाने की विधि-
बनाने की विधि-K2Cr2O7 को क्रोमाइट अयस्क (Fe2Cr2O4) या क्रोम आयरन (FeO.Cr203) से बनाया जाता है, जो निम्नलिखित पदों में होते हैं।
(1) क्रोमाइट अयस्क का सोडियम क्रोमेट में परिवर्तन-क्रोमाइट अयस्क को NaOH या Na2CO3 के साथ वायु की उपस्थिति में एक परावर्तनी भट्टी में गर्म करने पर सोडियम क्रोमेट (पीला रंग) बनता है।
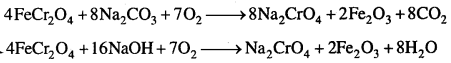
पदार्थ को छिद्रमय रखने हेतु कुछ मात्रा में शुष्क चूने को मिलाते हैं । जल के साथ निष्कर्षण करने पर Na2Cr2O3 विलयन में चला जाता है। जबकि Fe2O3 रह जाता है जिसे छानकर पृथक् कर लेते हैं।
(2) सोडियम क्रोमेट (Na2CrO4) का सोडियम डाइक्रोमेट (Na2Cr2O7) में परिवर्तन-सोडियम क्रोमेट विलयन सान्द्र H2SO4 के साथ अपचयित करके सोडियम डाइक्रोमेट बनाते हैं।
![]()
2Na2CrO4 कम विलेय होता है जिसका वाष्पन करने पर Na2SO410H2O के रूप में क्रिस्टलीकृत हो जाता है जिसे पृथक् कर लिया जाता है।
(3) Na2Cr2O7 का K2Cr2O7 में परिवर्तन-सोडियम डाइक्रोमेट के जलीय विलयन का उपचार KCI के साथ किये जाने पर पोटैशियम डाइ क्रोमेट प्राप्त होता है। K2Cr2O7 के अल्प विलेय प्रकृति के कारण इसके क्रिस्टल ठण्डे में प्राप्त किये जाते हैं।
![]()
K2Cr2O7 की निम्न के साथ होने वाली रासायनिक अभिक्रिया –
(1) अम्लीय फेरस सल्फेट के साथ-K2Cr207 अम्लीय माध्यम में यह फेरस सल्फेट को फेरिक सल्फेट में ऑक्सीकृत कर देता है। K2Cr2O7 पहले H2SO4 से क्रिया करके नवजात ऑक्सीजन का तीन परमाणु देता है जो Fe2+ को Fe3+ आयन में ऑक्सीकृत कर देता है।

pH बढ़ाने पर प्रभाव-पोटैशियम क्लोराइड सोडियम क्लोराइड से कम विलेयशील होता है। ये ऑरेंज क्रिस्टल के रूप में प्राप्त होते है तथा इन्हें फिल्ट्रेशन से हटाया जा सकता है। pH 4 पर डाइक्रोमेट आयन (CrO72-) क्रोमेट आयन CrO4 2-के रूप में उपस्थित होते हैं । ये pH के मान में परिवर्तन के अनुसार एक-दूसरे में परिवर्तनशील होते हैं।
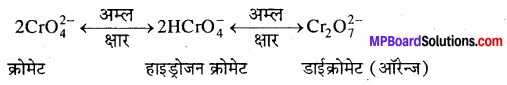
प्रश्न 15.
पोटैशियम डाइक्रोमेट की ऑक्सीकरण क्रियायें समझाइये एवं इनकी निम्न के साथ आयनिक अभिक्रियायें लिखिए
(i) आयोडाइड, (ii) आयरन (II) विलयन एवं (ii) H2S.
उत्तर
दीर्घ उत्तरीय प्रश्न 2 (K2Cr2O7 की निम्न के साथ होने वाली रासायनिक अभिक्रिया) देखें।
प्रश्न 16.
पोटैशियम परमैंगनेट के बनाने की विधि का वर्णन कीजिए।अम्लीकृत परमैंगनेट विलयन निम्न से कैसे क्रिया करता है
(i) आयरन (II) आयनों से, (ii) SO2 एवं (ii) ऑक्सेलिक अम्ल ? अभिक्रियाओं की आयनिक समीकरणों को लिखिए।
उत्तर
KMnO4, पायरोलुसाइट से बनाया जा सकता है, अयस्क को KOH के साथ वायुमण्डलीय ऑक्सीजन या ऑक्सीकृत एजेन्ट जैसे- KNO3 या KClO4 की उपस्थिति में क्रिया कराकर K2MnO4 प्राप्त किया जाता है।
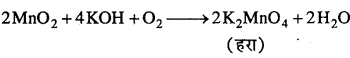
प्राप्त 2K2MnO4 (ग्रीन) को जल द्वारा छाना जा सकता है। फिर विद्युत्-अपघटन या क्लोरीन/ओजोन को विलयन मे प्रवाहित कर ऑक्सीकृत किया जाता है।
विद्युत्-अपघटनी ऑक्सीकरण –
2K2MnO4 ⇌ 2K+ + MnO42-
H2O → H+ + OH–
एनोड में मैंग्नेट आयन, पर मैंग्नेट आयन में ऑक्सीकृत होता है।
MnO42- → MnO4– + e –
क्लोरीन द्वारा ऑक्सीकरण –
2K2MnO4 + Cl2 → 2KMnO4 + 2KCl
2MnO42- + Cl2 → 2MnO–4 + 2Cl–
ओजोन द्वारा ऑक्सीकरण –
2K2MnO4 + O3 + H4O → 2KMnO4 + 2KOH + O2↑
2MnO42- + O3 +H2O → 2MnO42- + 2OH– + O2
अम्लीकृत KMnO4 विलयन Fe(II) आयन को Fe(III) आयन में ऑक्सीकृत करना है अर्थात् फेरस आयन से फेरिक आयन
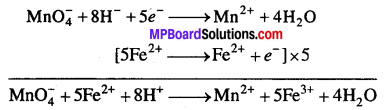
अम्लीकृत पोटैशियम परमैंग्नेट SO2 को H2SO4 में ऑक्सीकृत करता है।
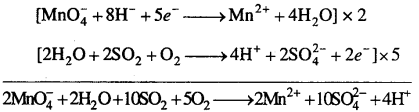
अम्लीकृत पोटैशियम परमैंग्नेट ऑक्सेलिक अम्ल को कार्बन डाइ-ऑक्साइड में ऑक्सीकृत करता है।
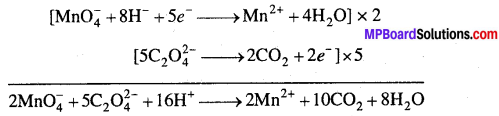
प्रश्न 17.
M22+M एवं M3+/M2+ तंत्रों के लिए कुछ धातुओं के E° मान निम्न है –
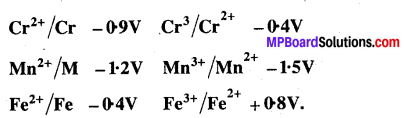
उपर्युक्त आँकड़ों का उपयोग कर निम्न पर टिप्पणी कीजिए –
(i) Cr3+ अथवा Mn3+ की तुलना में Fe3+ का अम्लीय विलयन में स्थायित्व एवं
(ii) वो कौन-सी स्थितियाँ हैं, जहाँ आयरन, समान विधियों में क्रोमियम अथवा मैंगनीज धातु की तुलना में ऑक्सीकृत होता है।
उत्तर
(i) जैसे- \(\mathrm{E}_{\mathrm{Cr}}^{\circ} / \mathrm{Cr}^{+2}\) ऋणात्मक (-04V) है, जिसका अर्थ है cr+3 आयन विलयन में सरलता से Cr+2 में अपचयित नहीं होता, अत: Cr+3 आयन अधिक स्थायी है। इसी प्रकार \(\mathrm{E}^{\circ}_{\mathrm{Mn}^{+} 3} / \mathrm{Mn}^{+2}\) धनात्मक (+1:5V) है, Mn+3 आयन सरलता से Mn+2 आयन में Fe+3 आयन की तुलना में अपचयित होता है अत: इन आयनों की आपेक्षिक स्थायित्व निम्न है –
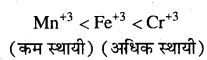
(ii) दिए गए जोड़ों का ऑक्सीकरण विभव +09V, +1-2V एवं 0-4V है। अत: इनके ऑक्सीकरण का क्रम निम्न है –
Mn>Cr>Fe
प्रश्न 18.
पहचानिए, निम्न में कौन जलीय विलयन में रंग देते हैं? Ti3+,V3+, Cu+,Sc3+,Mn2+, Fe3+ एवं CO2+ प्रत्येक का कारण दीजिए।
उत्तर
ऐसे आयन जिनमें एक या अधिक अयुग्मित इलेक्ट्रॉन होते हैं, जलीय विलयन में d – d संक्रमण के कारण रंगीन होते हैं।
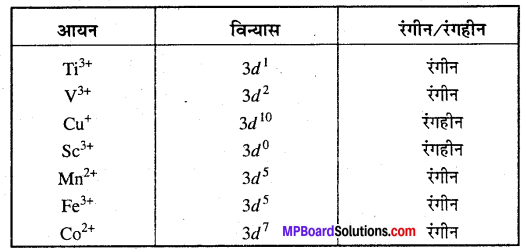
प्रश्न 19.
प्रथम संक्रमण श्रेणी के तत्वों की +2 ऑक्सीकरण अवस्था को स्थायित्व की तुलना कीजिए।
उत्तर
Mn एवं Zn को छोड़कर + 2 अवस्था का स्थायित्व बायें से दायें चलने पर घटता है। मानव अपचयन विभव के ऋणात्मक मान के घटने के कारण दाँयी तरफ स्थायित्व घटता है। कुल ∆1H1 + ∆1H2 (प्रथम एवं द्वितीय आयनन एन्थैल्पी में वृद्धि के कारण E° के ऋणात्मक मान कम होते हैं।)
प्रश्न 20.
निम्न को ध्यान में रखकर एक्टीनॉयड्स के रसायन की तुलना लैन्थेनॉयड्स के साथ कीजिए
(i) इलेक्ट्रॉनिक विन्यास
(ii) परमाणु एवं आयनिक आकार एवं
(iii) ऑक्सीकरण अवस्था
(iv) रासायनिक क्रियाशीलता।
उत्तर
लैंथेनाइडों एवं एक्टिनाइडों के मध्य भिन्नताएँ
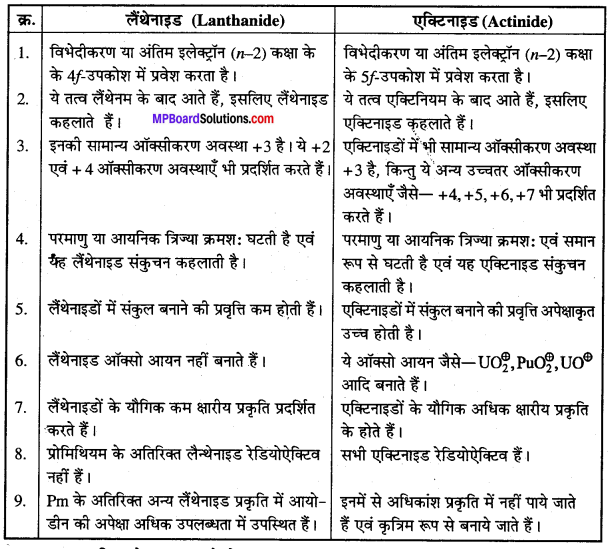
प्रश्न 21.
निम्न से क्या समझते हो –
(i) d4 श्रेणी में, Cr2+ प्रबल अपचायक है जबकि मैंगनीज (III) प्रबल ऑक्सीकारक है।
(ii) कोबाल्ट (II) जलीय विलयन में स्थायी है, जबकि जटिल अभिकर्मकों की उपस्थिति में यह आसानी से ऑक्सीकृत हो जाता है।
(iii) आयनों में d विन्यास अत्यधिक अस्थायी है।
उत्तर
(i) Cr2+ अपचायक प्रकृति का है, इसका विन्यास d4 से d3 (अर्द्धपूर्ण t.कक्षकों का स्थायी विन्यास) परिवर्तन होता है। अन्य शब्दों में Mn3+ ऑक्सीकारक प्रकृति का है, जिसका विन्यास d4 से d5 (अर्द्धपूर्ण t2g से 2g कक्षकों के स्थायी विन्यास) में परिवर्तन होता है।
(ii) प्रबल लिगेण्ड कोबाल्ट (II) को बल द्वारा 3d- उपकक्ष से एक अथवा अधिक इलेक्ट्रॉन को हटाता है, जिससे d2sp3 संकरण होता है।
(iii) d1-विन्यास वाला आयन प्रयास करता है कि d-उपकक्ष से एक इलेक्ट्रॉन निकालकर स्थायी अकिय गैस विन्यास प्राप्त कर लेवें।।
प्रश्न 22.
विषमसमानुपाती से क्या तात्पर्य है ? जलीय विलयन में विषमसमानुपाती अभिक्रिया के दो उदाहरण दीजिए।
उत्तर
विषमसमानुपाती अभिक्रियायें वे होती हैं, जिनमें समान पदार्थ ऑक्सीकृत एवं अपचयित होता है। उदाहरण के लिए –
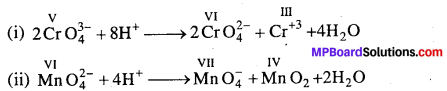
प्रश्न 23.
संक्रमण धातुओं की प्रथम श्रेणी की कौन-सी धातु सामान्य +1 ऑक्सीकरण अवस्था रखते हैं एवं क्यों ?
उत्तर
कॉपर का इलेक्ट्रॉनिक विन्यास [Ar]3d104s1 है। जो एक इलेक्ट्रॉन (4s1) सरलता से त्याग कर स्थायी विन्यास 3d10 देता है।
प्रश्न 24.
निम्न गैसीय आयनों में अयुग्मित इलेक्ट्रॉनों की गणना कीजिए- Mn3+, Cr3+,v3+ एवं Ti3+ इनमें से कोई एक जलीय विलयन में अधिक स्थायी है ?
उत्तर
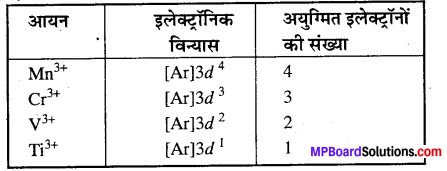
Cr2+ अत्यधिक स्थायी है, इसमें अर्द्धपूर्ण t2gस्तर होते हैं।
प्रश्न 25.
संक्रमण धातु रसायन के निम्न के उदाहरण एवं कारणों को दीजिए –
(i) संक्रमण धातु के निम्न ऑक्साइड क्षारीय हैं, उच्च उभयधर्मी/अम्लीय हैं।
(ii) संक्रमण धातु ऑक्साइडों एवं फ्लुओराइडों में उच्च ऑक्सीकरण अवस्था रखते हैं।
(iii) धातु ऑक्सो ऋणायनों में उच्च ऑक्सीकरण अवस्था होती है।
उत्तर
(i) संक्रमण तत्व के निम्न ऑक्साइड क्षारीय होते हैं, क्योंकि धातु परमाणुओं की निम्न
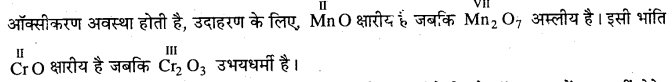
धातु की निम्न ऑक्सीकरण अवस्था में, धातु परमाणु के कुछ संयोजी इलेक्ट्रॉन बन्धन में भाग नहीं लेते। अत: ये इलेक्ट्रॉन को दानकर क्षार की भाँति व्यवहार करते हैं। उच्च ऑक्सीकरण अवस्था में, संयोजी इलेक्ट्रॉन बन्धन में भाग लेते हैं एवं जो उपलब्ध नहीं होते। इसके अतिरिक्त प्रभावी नाभिकीय आवेश अधिक होने पर यह इलेक्ट्रॉन स्वीकार करता है एवं अम्ल की भाँति व्यवहार दर्शाते हैं।
(ii) संक्रमण धातु ऑक्साइडों एवं फ्लुओराइडों में उच्च ऑक्सीकरण अवस्थायें रखते हैं, क्योंकि ऑक्सीजन एवं फ्लुओरीन का आकार छोटा एवं उच्च ऋणविद्युतता है एवं ये धातुओं को सरलता से ऑक्सीकृत करते हैं। उदाहरण के लिए- O5F6 [O5(VI)],V2O5 [v(v)] .
(iii) धातुओं के ऑक्सो ऋणायन उच्च ऑक्सीकरण अवस्थायें रखते हैं। उदाहरण के लिए, Cr2O72- में Cr की ऑक्सी-करण अवस्था + 6 है, जबकि MnO4– में Mn की ऑक्सी-करण अवस्था +7 है। क्योंकि ऑक्सीजन की उच्च ऋणविद्युतता एवं उच्च ऑक्सीकारक गुण है।
प्रश्न 26.
बनाने के पदों को दर्शाइये –
(i) क्रोमाइट अयस्क से K2Cr2O7
(ii) पायरोलुसाइट अयस्क से KMnO4.
उत्तर
दीर्घ उत्तरीय प्रश्न क्र. 2 एवं 4 देखें।
प्रश्न 27.
मिश्रधातुएँ क्या हैं ? प्रमुख मिश्रधातु के नाम लिखते हुए उसके उपयोग लिखिए, जिनमें कुछ लैन्थेनॉयड्स धातुएँ होती हैं।
उत्तर
दो अथवा अधिक धातुओं अथवा धातुओं एवं अधातुओं के समांगी मिश्रण मिश्रधातु है । प्रमुख मिश्रधातु जिसमें लैन्थेनॉयड होता है, मिश्रधातु है, जिसमें 95% लैन्थेनॉयड धातुएँ एवं 5% आयरन के साथ थोड़ी मात्रा में S, C, Ca एवं Al होते हैं । इसका उपयोग Mg-आधारित मिश्रधातु में करते हैं। जो गोली के आवरण एवं लाइटर में उपयोग होती है।
प्रश्न 28.
अन्तर संक्रमण तत्व क्या हैं ? दिए गए निम्न परमाणु संख्याओं में से अन्तर संक्रमण तत्वों की परमाणु संख्याओं का निर्धारण कीजिए- 29,59, 74, 95, 102, 104.
उत्तर
f-ब्लॉक तत्वों में, अन्तिम इलेक्ट्रॉन अन्तर उपात्यकक्ष – उपकक्ष में प्रवेश करते हैं, अतः इन्हें अन्तर संक्रमण तत्व कहते हैं। इनमें लैन्थेनॉयड्स (58-71) एवं एक्टीनॉयड्स (90-103) होते हैं । अतः परमाणु क्रमांक 59, 95 एवं 102 वाले तत्व अन्तर संक्रमण तत्व हैं।
प्रश्न 29.
लैन्थेनॉयड्स की तुलना में एक्टीनॉयड्स तत्वों का रसायन अधिक सरल नहीं है। इस वाक्य को इन तत्वों की ऑक्सीकरण अवस्था के कुछ उदाहरणों द्वारा न्यायोचित सिद्ध कीजिए।
उतर
लैन्थेनॉयड्स निश्चित संख्या में ऑक्सीकरण अवस्थायें दर्शाते हैं, जैसे +2, +3 एवं +4 (+3 मुख्य ऑक्सीकरण अवस्था है)। क्योंकि 5d एवं 4f उपकक्षों के मध्य अधिक ऊर्जा अन्तर होता है। एक्टीनॉयड्स भी प्रमुख ऑक्सीकरण अवस्था +3 दर्शाते हैं, किन्तु अन्य ऑक्सीकरण अवस्था भी दर्शाते हैं । उदाहरण के लिए, यूरेनियम (Z= 92) +3, +4, +5, +6 ऑक्सीकरण अवस्थायें रखता है, एवं नेप्चूनियम (Z= 94) +3, +4, +5, +6 एवं +7 ऑक्सीकरण अवस्थायें दर्शाता है। क्योंकि 4f एवं 6d कक्षकों के मध्य ऊर्जा अन्तर कम होता है।
प्रश्न 30.
एक्टीनॉयड्स श्रेणी का अंतिम तत्व कौन-सा है ? इस तत्व का इलेक्ट्रॉनिक विन्यास लिखिए। इस तत्व की संभावित ऑक्सीकरण अवस्था पर टिप्पणी कीजिए।
उत्तर
एक्टीनॉयड श्रेणी का अंतिम तत्व= लॉरेन्सियम (Z = 103)
इलेक्ट्रॉनिक विन्यास = [Rn]5f146d17s2
संभावित ऑक्सीकरण अवस्था = +3
प्रश्न 31.
हुण्ड नियम का उपयोग करते हुए Ce* आयन का इलेक्ट्रॉनिक विन्यास लिखिए एवं ‘चक्रण केवल’ सूत्र के आधार पर इसके चुम्बकीय आघूर्ण की गणना कीजिए।
उत्तर
सीरियम का इलेक्ट्रॉनिक विन्यास = [Xe] 4f15d16s2
Ce3+ 344 = [Xe]4f1
जिसका अर्थ है कि एक अयुग्मित इलेक्ट्रॉन उपस्थित है।
![]()
प्रश्न 32.
लैन्थेनॉयड श्रेणी के उन सदस्यों के नाम दीजिए, जो +4 ऑक्सीकरण अवस्था में एवं +2 ऑक्सीकरण अवस्थायें रखते हैं। इस प्रकार के व्यवहार को इन तत्वों के इलेक्ट्रॉनिक विन्यासों से संबंध स्थापित कीजिए।
उत्तर
+4= 58Ce, 59Pr, 60Nd, 65Tb, 66Dy
+2 = 60Nd, 62Sm, 63Eu, 69Tm, 70Yb
+4 ऑक्सीकरण अवस्था दर्शाती है, जब विन्यास बाँयी तरफ के समीप 4f° (अर्थात् 4f04f14f2) अथवा 4f7 के समीप (अर्थात् 4f7 अथवा 4f8) होता है।
+2 ऑक्सीकरण अवस्था दर्शाती है, जब विन्यास 5d0 6s2 है तथा दो इलेक्ट्रॉन सरलता से त्याग देता है।
प्रश्न 33.
निम्न के सापेक्ष एक्टीनॉयड्स एवं लैन्थेनॉयड्स के रसायन की तुलना कीजिए –
(i) इलेक्ट्रॉनिक विन्यास
(ii) ऑक्सीकरण अवस्थाएँ
(iii) आयनन एन्थैल्पी एवं
(iv) परमाण्विक आकार।
उत्तर
लैंथेनाइडों एवं एक्टिनाइडों के मध्य भिन्नताएँ
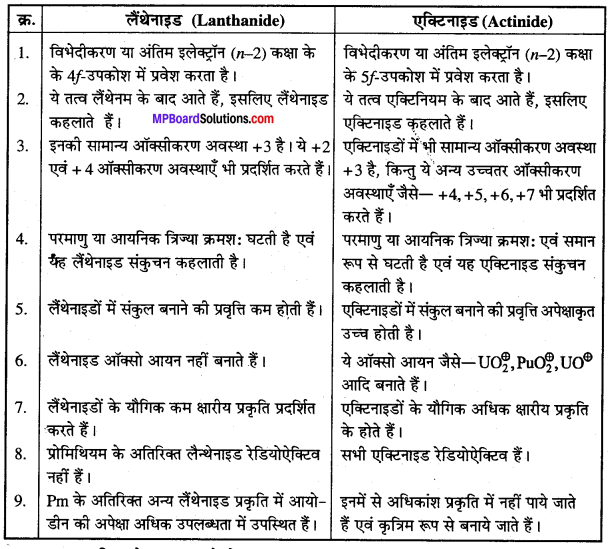
प्रश्न 34.
परमाणु क्रमांक 61,91, 101 एवं 109 वाले तत्वों के इलेक्ट्रॉनिक विन्यास लिखिए।
(i) z = 61: [Xe]4f5f506s2
(ii) Z = 91: [Rn]5f26d17s2
(iii) Z = 101: [Rn]5f136d07s2
(iv) Z = 109: [Rn]5f146d7s2
प्रश्न 35.
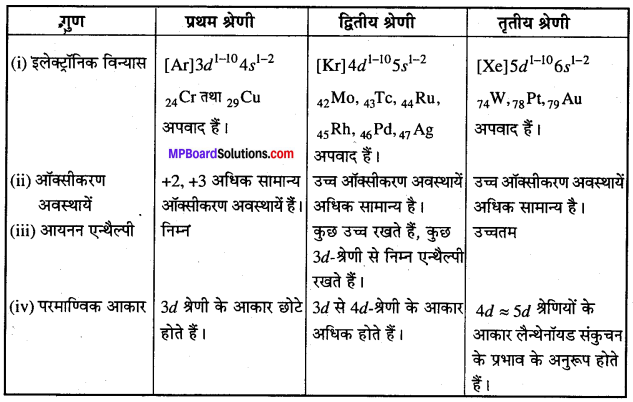
ऊर्ध्वाधर कॉलम के सापेक्ष प्रथम संक्रमण धातुओं की श्रेणी के सामान्य गुणों की तुलना द्वितीय एवं तृतीय श्रेणी के धातुओं से कीजिए। निम्न बिन्दुओं को विशिष्टता प्रदान कीजिए –
(i) इलेक्ट्रॉनिक विन्यास,
(ii) ऑक्सीकरण अवस्थायें
(iii) आयनन एन्थैल्पी एवं
(iv) परमाण्विक आकार।
उत्तर
प्रथम संक्रमण धातुओं की श्रेणी के सामान्य गुणों की तुलना –
प्रश्न 36.
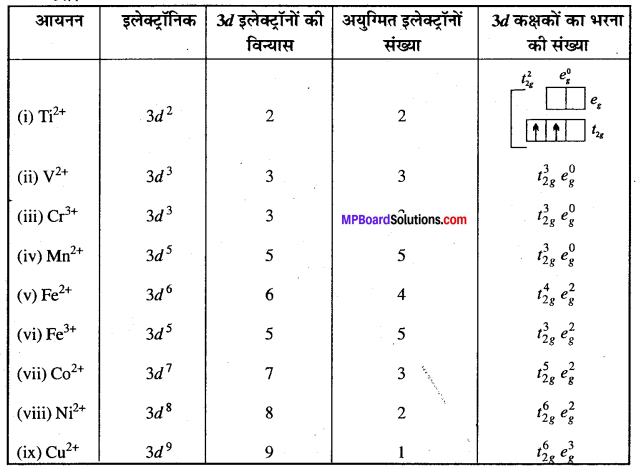
निम्न आयनों में प्रत्येक के 3d इलेक्ट्रॉनों की संख्या लिखिए –
Ti2+,v2+, Cr3+,Mn2+, Fe2+, Fe3+,Co2+,Ni2+ एवं Cu2+ दर्शाइये कि पाँच 31 कक्षकों को इन हाइड्रेट आयनों (अष्टफलकीय) द्वारा भरा जा सकता है।
उत्तर
प्रश्न 37.
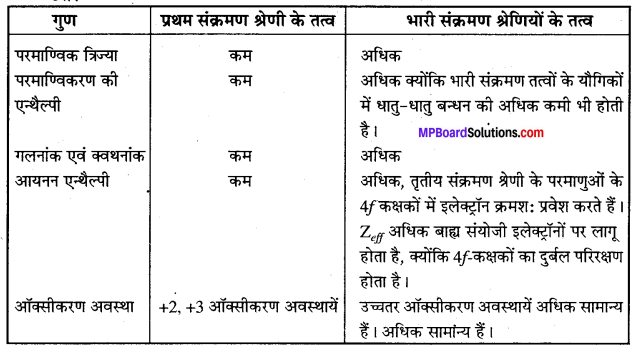
इस वाक्य पर टिप्पणी कीजिए कि प्रथम संक्रमण श्रेणी के तत्वों में अनेक गुण भारी संक्रमण तत्वों से भिन्न होते हैं।
उत्तर
प्रश्न 38.
निम्न संकुल स्पीशीज के चुम्बकीय आघूर्ण के मानों से क्या दर्शाया जाता है ?
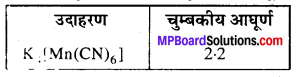
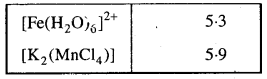
उत्तर
K4[Mn(CN)6]
Mn+2 . 3d5 , चुम्बकीय आघूर्ण 2.2 दर्शाता है कि इसमें एक अयुग्मित इलेक्ट्रॉन है एवं अन्तर कक्षक संकुल अथवा निम्न चक्रण संकुल बनाता है। इसका विन्यास है –
t22g[Fe(H2 O)6 ]2+
Fe+2: 3d6 चुम्बकीय आघूर्ण का मान 4 अयुग्मित इलेक्ट्रॉनों के समीप है, अत: यह बाह्य कक्षक संकुल अथवा उच्च चक्रण संकुल बनाता है। इसका विन्यास है – t42g e2g K2[MnCl4]
Mn+2 : 3d5 चुम्बकीय आघूर्ण का मान 5 अयुग्मित इलेक्ट्रॉनों के सापेक्ष है। d-कक्षक प्रभावित नहीं होते। अतः यह चतुष्फलकीय संकुल बनाता है। इसका विन्यास है – t32g e2g
d एवं f-ब्लॉक के तत्त्व अन्य महत्वपूर्ण प्रश्नोत्तर
d एवं f-ब्लॉक के तत्त्व वस्तुनिष्ठ प्रश्न
1. सही विकल्प चुनकर लिखिए-
प्रश्न 1.
मैंगनीज किसमें उच्चतम ऑक्सीकरण अवस्था प्रदर्शित करता है
(a) K2MnO4
(b) KMnO4
(c) MnO2
(d) MngO4
उत्तर
(b) KMnO4
प्रश्न 2.
कौन अन्तराली यौगिक बनाता है
(a) Fe
(b) Ca
(c) Ni
(d) सभी।
उत्तर
(b) Ca
प्रश्न 3.
जब KMnO4 को उदासीन माध्यम में प्रयुक्त करते हैं, तब उनका तुल्यांक भार होगा –
(a) M
(b) M/2
(c) M/3
(d) M/5.
उत्तर
(c) M/3
प्रश्न 4.
कौन-सी लैन्थेनाइड सर्वाधिक प्रयुक्त की जाती है –
(a) लैन्थेनम
(b) नोबेलियम
(c) थोरियम
(d) सीरियम।
उत्तर
(d) सीरियम।
प्रश्न 5.
गैडोलिनियम का इलेक्ट्रॉनिक विन्यास है –
(a) [Xc]4f65d9,6s2
(b) [Xe]4f7,5d1,6s2
(C) [Xe] f3,5d5,6s2
(d) [Xe]4f6,5d2,6s2.
उत्तर
(b) [Xe]4f7,5d1,6s2
प्रश्न 6.
लैन्थेनाइड संकुचन निम्न कारक के लिए उत्तरदायी होता है –
(a) Zr एवं Y की त्रिज्या लगभग समान होती है
(b) Zr एवं Nb की ऑक्सीकरण अवस्था समान होती है
(c) Zr एवं Hf की त्रिज्या लगभग समान होती है
(d)zr एवं Zn की ऑक्सीकरण अवस्था समान होती है।
उत्तर
(c) Zr एवं Hf की त्रिज्या लगभग समान होती है
प्रश्न 7.
3d श्रेणी में उच्चतम ऑक्सीकरण अवस्था किसके द्वारा प्रदर्शित की जाती है –
(a) Mn
(b) Fe2+
(c) Ni
(d) Cr
उत्तर
(a) Mn
प्रश्न 8.
कौन-सा संक्रमण धातु आयन रंगीन है –
(a) Cu+
(b) v2+
(c) Sc+3
(d) Ti+4
उत्तर
(b) v2+
प्रश्न 9.
एक संक्रमण धातु जो +3 ऑक्सीकरण अवस्था में हरा किन्तु +6 ऑक्सीकरण अवस्था में नारंगी होता है –
(a) Mn.
(b) Cr
(c) Os
(d) Fe.
उत्तर
(b) Cr
प्रश्न 10.
लैन्थेनाइड श्रेणी में, लैन्थेनाइड हाइड्रॉक्साइडों की क्षारकता –
(a) बढ़ती है
(b) घटती है
(c) पहले बढ़ती है फिर घटती है
(d) पहले घटती है और फिर बढ़ती है।
उत्तर
(b) घटती है
प्रश्न 11.
Fe, Co, Ni किस प्रकार के चुम्बकीय पदार्थ हैं –
(a) अनुचुम्बकीय
(b) लौह चुम्बकीय
(c) प्रति चुम्बकीय
(d) प्रति लौह चुम्बकीय।
उत्तर
(b) लौह चुम्बकीय
प्रश्न 12.
Fe+2 आयन के अयुग्मित इलेक्ट्रॉन की संख्या है –
(a) 0
(b) 4
(c) 6
(d) 3.
उत्तर
(b) 4
2. रिक्त स्थानों की पूर्ति कीजिए –
- Fe, Co, Ni धातुओं को …………. कहते हैं।
- परमाणु क्रमांक में वृद्धि के साथ त्रिसंयोजी धनायनों का आकार क्रमशः….,.. जाता है।
- निम्नतर ऑक्सीकरण अवस्था प्रदर्शित करने वाले संक्रमण धातु …….. प्रकृति के होते हैं।
- K2Cr207 एक प्रबल ……….. है जो केवल अम्लीय माध्यम में नवजात ऑक्सीजन का ……… परमाणु मुक्त करता है।
- Zn केवल …………. ऑक्सीकरण अवस्था प्रदर्शित करता है।
- f-ब्लॉक तत्व …………. तत्व कहलाते हैं।
- संक्रमण तत्व और उनके यौगिक ……….. का कार्य करते हैं।
- अंतः संक्रमण तत्वों का सामान्य इलेक्ट्रॉनिक विन्यास …………..
- पोटैशियम मैंगनेट का रासायनिक सूत्र ……….. है।
- d-ब्लॉक तत्वों को …………. भी कहा जाता है।
उत्तर
- फेरस धातुएँ
- घटता
- क्षारीय
- ऑक्सीकारक, तीन
- +2
- आन्तर संक्रमण
- उत्प्रेरक
- (n-2)f1-14, (n-1)d1-2,ns2
- K2MnO4,
- संक्रमण तत्व।
3. सत्य/असत्य बताइए –
- पारा द्रव अवस्था में होता है तथा इसकी ऑक्सीकरण अवस्था +1 व + 2 होती है।
- संक्रमण धातुओं की उच्चतम ऑक्सीकरण अवस्था अम्लीय प्रकृति की होती है।
- लैन्थेनाइड और एक्टीनाइड दोनों संक्रमण तत्व कहलाते हैं।
- सभी संक्रमण तत्वों में +2 ऑक्सीकरण अवस्था सामान्यत: अधिक पायी जाती है अथवा सामान्य होती है।
- Zn, Cd एवं Hg परिवर्ती संयोजकता प्रदर्शित करती है।
- Cu+2 आयन रंगहीन और प्रतिचुम्बकीय होता है।
- प्लूटोनियम का उपयोग परमाणु बम बनाने में तथा परमाणु रियेक्टर में ईंधन के रूप में किया जाता है।
- संक्रमण तत्व अन्तराली यौगिक बनाते हैं।
उत्तर
- सत्य,
- सत्य,
- असत्य,
- सत्य,
- असत्य,
- असत्य,
- सत्य,
- सत्य।
4. उचित संबंध जोडिए –
I.

उत्तर
1. (1), 2. (g), 3. (e), 4. (c), 5. (b), 6, (d), 7. (a).
5. एक शब्द/वाक्य में उत्तर दीजिए –
- Cu+ तथा Cu2+ में कौन-सा आयन रंगहीन है ?
- एक अभिक्रिया में KMnO4 को K2MnO4 में परिवर्तित किया जाता है तो Mn की ऑक्सी
करण संख्या में कितना परिवर्तन होगा? - लैन्थेनाइड और एक्टीनाइड में कौन-सी श्रेणी उच्च ऑक्सीकरण अवस्था दर्शाती है ?
- लैन्थेनम की कौन-सी ऑक्सीकरण अवस्था अधिक स्थायी होती है ?
- K3Cr3O7 का अम्लीय विलयन में तुल्यांकी भार कितना होता है ?
- Fe+3 में अयुग्मित इलेक्ट्रॉनों की अधिकतम संख्या होती है।
- क्रोमिलं क्लोराइड परीक्षण में प्रयुक्त ऑक्सीकरण का नाम लिखिए।
- d- ब्लॉक के तत्वों में Zn परिवर्तित संयोजकता प्रदर्शित नहीं करता, क्योंकि।
- Cu की सर्वाधिक महत्वपूर्ण ऑक्सीकरण अवस्था है।
- f- ब्लॉक के तत्वों को कितने श्रेणी में बाँटा गया है ?
- लूनर कॉस्टिक किसे कहते हैं ?
- d-ब्लॉक के तत्वों में Zn परिवर्ती ऑक्सीकरण संख्या नहीं दर्शाता है, क्यों ?
- HgCl2 तथा KI का क्षारीय विलयन क्या कहलाता है ?
उत्तर-
- Cu+
- 1,
- एक्टीनाइड,
- +3,
- 49,
- 5,
- K2Cr2O7,
- पूर्ण-पूरित d-कक्षक,
- +2,
- दो,
- AgNO3,
- d-कक्षक के पूर्ण भरे होने की वजह से,
- नेसलर अभिकर्मक।
d एवं f-ब्लॉक के तत्त्व लघु उत्तरीय प्रश्न
प्रश्न 1.
सिल्वर परमाणु की मूल अवस्था में पूर्ण-पूरित d-कक्षक है।आप कैसे कह सकते हैं कि यह एक संक्रमण तत्व है ?
उत्तर
सिल्वर +1 ऑक्सीकरण अवस्था में 4d10 5s0 इलेक्ट्रॉनिक विन्यास दर्शाता है। परन्तु कुछ यौगिकों में यह +2 ऑक्सीकरण अवस्था दर्शाता है। इस अवस्था में यह 4d95s0 इलेक्ट्रॉनिक विन्यास दर्शाता है। अतः 4d- से कक्षक के अपूर्ण होने के कारण इसे संक्रमण तत्व माना गया है।
प्रश्न 2.
संक्रमण तत्व किसे कहते हैं ? इनका इलेक्ट्रॉनिक विन्यास लिखिए। ये धात्विक गुण प्रदर्शित करते हैं, क्यों?
उत्तर
वे तत्व, जिनके परमाणु अथवा साधारण आयनों के इलेक्ट्रॉनिक विन्यास में भीतरी d-कक्षक अपूर्ण रूप से भरे होते हैं, संक्रमण तत्व कहलाते हैं । ये समूह 2 और 13 के मध्य स्थित होते हैं।
उदाहरण-Fe, Ni, Co आदि। इलेक्ट्रॉनिक विन्यास-(n-1)1-10,ns1-2 है।
किसी तत्व द्वारा अपने परमाणु में से एक अथवा अधिक इलेक्ट्रॉन त्यागकर धनायन बनाने की क्षमता पर उसका धात्विक गुण निर्भर करता है, सभी संक्रमण तत्व धातुएँ हैं, क्योंकि इनकी बाह्यतम कक्षा में एक या दो इलेक्ट्रॉन होते हैं, जो कि आसानी से त्यागे जा सकते हैं, क्योंकि इनकी आयनन ऊर्जा निम्न होती है। अतः ये धात्विक प्रकृति के होते हैं।
प्रश्न 3.
संक्रमण तत्व परिवर्ती संयोजकता प्रदर्शित करते हैं, क्यों?
उत्तर-
संक्रमण तत्व परिवर्ती संयोजकता प्रदर्शित करते हैं, क्योंकि (n-1)d-कक्षक तथा ns-कक्षक के इलेक्ट्रॉनों की ऊर्जा में बहुत अधिक अन्तर नहीं होता है, जिससे d-कक्षक के इलेक्ट्रॉन भी संयोजी इलेक्ट्रॉन का कार्य करते हैं । इन तत्वों में Mn अधिकतम परिवर्ती संयोजकता प्रदर्शित करता है।
प्रश्न 4.
संक्रमण धातुएँ आसानी से मिश्र धातुएँ क्यों बना लेती हैं ?
उत्तर
संक्रमण धातुएँ पिघली हुई अवस्था में एक-दूसरे में मिश्रणीय हैं तथा विभिन्न संक्रमण धातुओं के मिश्रण को ठण्डा करने पर मिश्र धातुएँ बनती हैं । संक्रमण धातुओं का आकार लगभग समान होता है, अतः क्रिस्टल जालक में एक धातु परमाणु को दूसरे धातु परमाणु से आसानी से विस्थापित किया जा सकता है, इस प्रकार मिश्रधातुएँ बनती हैं । जैसे-Cr को Ni में विलेय कर Cr-Ni मिश्रधातु बनाया जाता है। मिश्र धातुएँ अपनी जनक धातुओं की तुलना में अधिक कठोर, उच्च गलनांक वाली तथा अधिक संक्षारण प्रतिरोधी होती हैं।
प्रश्न 5.
संक्रमण धातुओं के चुम्बकीय गुणों को उसके इलेक्ट्रॉनिक विन्यास के आधार पर बताइए।
अथवा, अनुचुम्बकत्व और प्रतिचुम्बकत्व को समझाइए।
उत्तर
चुम्बकीय गुण-संक्रमण धातुएँ चुम्बकीय गुण प्रदर्शित करती हैं।
(a) प्रतिचुम्बकत्व-जब किसी पदार्थ में उपस्थित सभी इलेक्ट्रॉन युग्मित हों तो वह प्रतिचुम्बकत्व दर्शाता है। Zn एक प्रतिचुम्बकीय धातु है।
(b) अनुचुम्बकत्व-यह गुण पदार्थ में उपस्थित अयुग्मित इलेक्ट्रॉनों की संख्या पर निर्भर करता है। अयुग्मित इलेक्ट्रॉन युक्त पदार्थ अनुचुम्बकीय होता है । अयुग्मित इलेक्ट्रॉनों की संख्या बढ़ने से चुम्बकीय गुण भी बढ़ता है।
Fe, Co तथा Ni फेरोचुम्बकीय होते हैं, क्योंकि इन्हें चुम्बकित भी किया जा सकता है । अनुचुम्बकत्व को निम्न सूत्र से दर्शाते हैं –
![]()
जिसमें μ = चुम्बकीय आघूर्ण, n = अयुग्मित इलेक्ट्रॉनों की संख्या।
प्रश्न 6.
संक्रमण तत्वों की प्रवृत्ति अक्रिय होती है, क्यों? उत्तर
संक्रमण तत्वों की अक्रिय प्रवृत्ति या कम क्रियाशीलता निम्नलिखित कारणों से होती हैं –
(i) इनके मानक इलेक्ट्रोड विभव का मान कम होता है ।
(ii) इनकी आयनन ऊर्जा उच्च होती है ।
(iii) इनकी वाष्पन या कणिकरण ऊर्जा (Sublimation of Atomization energy) का मान उच्च होता है।
(iv) इनके आयनों की जल योजन ऊर्जा का मान कम होता है ।
प्रश्न 7.
संक्रमण तत्वों की विशेषताएँ लिखिए।
उत्तर
संक्रमण तत्वों की विशेषताएँ-
- इनकी प्रकृति धात्विक होती है जिनका धन विद्युतीय गुण सीमित (Ti) से उत्कृष्ट (Cu) तक होता है।
- ये कठोर होते हैं तथा ऊष्मा और विद्युत् के सुचालक हैं।
- इनके b.p. तथा m.p. उच्च होते हैं ।
- ये परिवर्ती ऑक्सीकरण अवस्था प्रदर्शित करते हैं ।
- ये रंगीन आयन बनाते हैं ।
- ये समन्वयन यौगिक बनाते हैं।
- ये सामान्यत: अनुचुम्बकीय होते हैं ।
- ये अच्छे उत्प्रेरक होते हैं।
- ये मिश्रधातु बनाते हैं।
- ये अधातुओं के साथ अन्तराकाशीय यौगिक बनाते हैं।
- इनमें कार्बधात्विक यौगिक, समाकृतिक यौगिक तथा नॉन-स्टॉइकियोमीट्रिक यौगिक भी पाये जाते हैं। __
प्रश्न 8.
d और f-ब्लॉक तत्वों में कोई पाँच प्रमुख अन्तर दीजिए।
उत्तर
d और ब्लिॉक तत्वों में अन्तर –
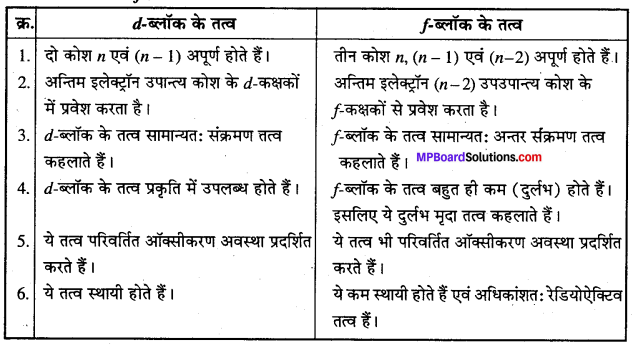
प्रश्न 9.
आन्तरिक संक्रमण तत्व क्या होते हैं ?
उत्तर
वे तत्व जिनमें तीनों बाह्यतम कोश अपूर्ण भरे होते हैं अन्तर संक्रमण तत्व कहलाते हैं। संक्रमण तत्वों के भीतर वर्ग 3 व 4 के मध्य 14-14 तत्व f-ब्लॉक में आते हैं। अतः संक्रमण तत्वों के मध्य स्थित होने के कारण इन्हें अन्तर संक्रमण तत्व कहते हैं। चूँकि इनमें अंतिम इलेक्ट्रॉन बाह्यतम कोश से दो अन्दर के कोश उपउपान्त्य कोश अर्थात् (n-2)f-ऑर्बिटल में प्रवेश करते हैं। अत: इन तत्वों को f-ब्लॉक तत्व भी कहते हैं। (n-2)f1-14(n-12)d1-10ns2 इन्हें दो श्रेणियों में बाँटा गया है –
(1) लैन्थेनाइड श्रेणी-लैन्थेनम के बाद (La57) आने वाले 14 तत्व (Ce58-Lu71) लैन्थेनाइड कहलाते हैं।
(2) ऐक्टिनाइड श्रेणी-ऐक्टिनम के बाद आने वाले 14 तत्व ऐक्टिनाइड्स कहलाते हैं।
प्रश्न 10.
समूह- 12 के सदस्यों के नाम लिखिए। वे सामान्यतः संक्रमण तत्व क्यों नहीं माने जाते हैं ?
उत्तर
समूह- 12 के सदस्यों के नाम Zn, Cd, Hg हैं जिन्हें संक्रमण तत्वों में शामिल नहीं किया गया है, क्योंकि इनकी परमाणु अवस्था तथा द्विसंयोजी आयन अवस्था दोनों में इलेक्ट्रॉनिक संरचना (n-1)d10 होती है अर्थात् इनके d- कक्षक पूर्णतः भरे होते हैं। इस कारण इन्हें संक्रमण तत्व नहीं माना जाता।
प्रश्न 11.
लैन्थेनाइडों की पाँच विशेषताएँ लिखिए। उत्तर-लैन्थेनाइडों की विशेषताएँ –
(a) ये f-ब्लॉक के तत्व हैं ।
(b) ये चाँदी के समान चमकदार धातुएँ हैं ।
(c) ये ऊष्मा तथा विद्युत् के अच्छे चालक हैं ।
(d) इनका गलनांक तथा घनत्व उच्च होता है ।
(e) La से Lu तक इनकी परमाणु त्रिज्या में लगातार कमी होती है, इसे लैन्थेनाइड संकुचन कहते हैं ।
प्रश्न 12.
क्या कारण है कि 5d श्रेणी के तत्वों की आयनन ऊर्जा का मान 4d श्रेणी से अधिक होता है?
उत्तर
किसी समूह में ऊपर से नीचे जाने पर आयनन ऊर्जा का मान घटता है, लेकिन अपेक्षा के विरुद्ध 5d श्रेणी के संक्रमण तत्वों की आयनन ऊर्जा का मान 4d श्रेणी के तत्वों के मान से अधिक होता है, जिसका कारण इन दोनों श्रेणियों के बीच आने वाले 14 लैन्थेनाइड तत्वों का रहना तथा उनके आकार में अपेक्षित वृद्धि नहीं हो पाना है। अतः नाभिक का आकर्षण बल बाह्यतम कक्षा के इलेक्ट्रॉन के लिए अधिक हो जाता है यही उनके अधिक आयनन विभव का कारण है।
प्रश्न 13.
(i) संक्रमण धातुओं में संकुल यौगिक बनाने की प्रवृत्ति होती है। समझाइए।
(ii) Zn, Cd एवं Hg संक्रमण तत्व का गुण व्यक्त क्यों नहीं करते हैं ?
(iii) Ti को आश्चर्यजनक धातु क्यों कहते हैं ?
उत्तर
(i) संक्रमण तत्वों के संकुल यौगिक बन्गने के कारण –
1. इन तत्वों के आयनों का आकार कम तथा नाभिकीय आवेश उच्च होता है, जिसके कारण ये आयन या अणु (लिगण्ड) को अपनी ओर आकर्षित करते हैं।
2. लिगैण्ड द्वारा दिये जाने वाले इलेक्ट्रॉन युग्म को ग्रहण करने के लिए इन तत्वों के आयनों में रिक्त ऑर्बिटल होते हैं।
(ii) ऐसे तत्व जिनमें (n-1)d- उपकोश आंशिक (Partially) रूप से भरे रहते हैं, उन्हें संक्रपण तत्व कहते हैं।
जबकि Zn में [3d104s2], Cd में [4d10 5s2] एवं Hg में [5d10s2] अवस्था पायी जाती है। इसलिए इन्हें संक्रमण तत्व नहीं मानते हैं।
(iii) Ti को आश्चर्यजनक धातु कहते हैं क्योंकि – (1) यह कठोर व उच्च गलनांक वाली धातु है। (2) यह ऊष्मा व विद्युत् की सुचालक होती है। (3) संक्षारण प्रतिरोधी होती है।(4) इसका उपयोग टैंक, तोप, बन्दूक व रक्षात्मक कवच बनाने में किया जाता है।
प्रश्न 14.
Fe2+ आयन की त्रिज्या Mn2+ आयन की त्रिज्या से कम होती है, क्यों?
उत्तर
Fe का परमाणु क्रमांक (26) Mn के परमाणु क्रमांक (25) से अधिक है। अधिक परमाणुक्रमांक होने से नाभिक में प्रोटॉन की संख्या अधिक होती है, फलतः नाभिक और बाह्य कोश के इलेक्ट्रॉन के बीच कार्य करने वाला आकर्षण बल उतना ही प्रबल होता है। प्रबल आकर्षण बल इलेक्ट्रॉन बल इलेक्ट्रान मेघ को भीतर की ओर खींचता है, जिससे आकार में कमी होती है, इसीलिए Fe+ आयन की त्रिज्या Mn2+ आयन से कम होती है।
प्रश्न 15.
लैन्थेनाइड समूह को पृथक् करना क्यों कठिन है ? समझाइए।
उत्तर
लैन्थेनाइड समूह (Ce58 से – 71Lu) तक तत्वों में लैन्थेनाइड संकुचन के कारण रासायनिक गुणों में अत्यधिक समानता होती है। अत: इन्हें शुद्ध अवस्था में प्राप्त करना अत्यधिक कठिन होता है। इन्हें आयन विनिमय विधि द्वारा पृथक् किया जाता है।
प्रश्न 16.
(i) TiO2 श्वेत है, जबकि TiCl3 बैंगनी है। क्यों?
(ii) संक्रमण धातुओं की प्रथम पंक्ति में Cr तक अनुचुम्बकत्व बढ़ता है और फिर घटने लगता है, क्यों?
उत्तर
(i) TiO2 में Ti4+ अवस्था में है जिसका इलेक्ट्रॉनिक विन्यास 3d0 है अतःd-इलेक्ट्रॉन के अभाव में d-d संक्रमण नहीं हो पाने के कारण TiO2 श्वेत है। जबकि TiCl3 में Ti3+ अवस्था में है जिसका विन्यास 3d1 है। अतः अयुग्मित d-इलेक्ट्रॉन की उपस्थिति के कारण TiCl3 बैंगनी रंग का होता है।
(ii) संक्रमण धातुओं की प्रथम पंक्ति में Cr (3d5) तक अयुग्मित d-इलेक्ट्रॉनों के संख्या में वृद्धि होती है तथा फिर युग्मन प्रारम्भ होने के कारण इनकी संख्या घटती जाती है। अत: इसी के अनुसार पहले Cr तक अनुचुम्बकत्व बढ़ता है और फिर घटने लगता है।
प्रश्न 17.
किन्हीं पाँच बिन्दुओं पर लैन्थेनाइड और ऐक्टिनाइड की तुलना कीजिए।
उत्तर-लैन्थेनाइडों एवं ऐक्टिनाइडों की तुलना –
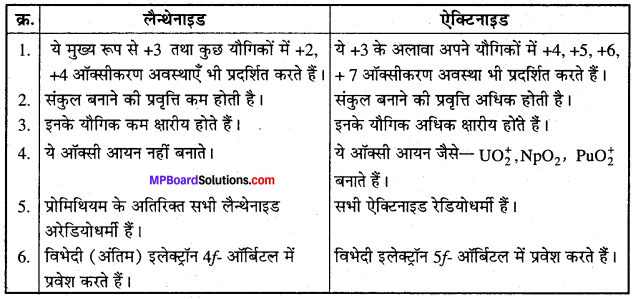
प्रश्न 18.
क्रोमिल क्लोराइड परीक्षण समीकरण सहित लिखिए।
उत्तर
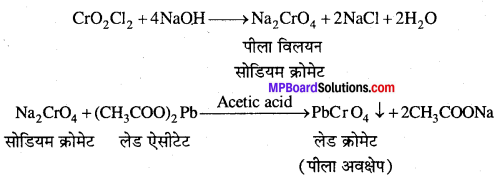
जब किसी धातु क्लोराइड को ठोस पोटैशियम डाइक्रोमेट एवं सांद्र H,SO के साथ गर्म किया जाता है तब क्रोमिल क्लोराइड का नारंगी वाष्प बनता है।
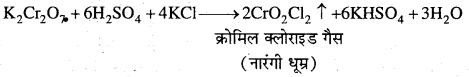
प्राप्त वाष्प को NaOH विलयन में प्रवाहित करने पर सोडियम क्रोमेट का पीले रंग का विलयन प्राप्त होता है, जो CH3COOH की उपस्थिति में लेड ऐसीटेट मिलाने पर, लेड क्रोमेट का पीला अवक्षेप देता है।
प्रश्न 19.
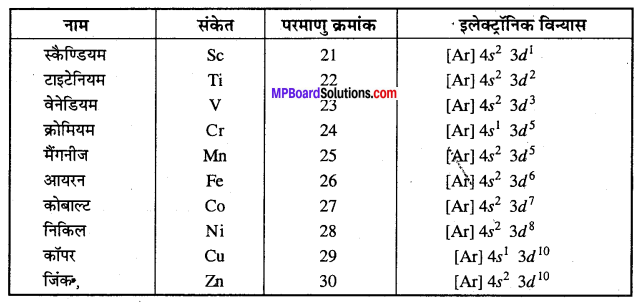
प्रथम संक्रमण श्रेणी में उपस्थित तत्वों के नाम, संकेत तथा इलेक्ट्रॉनिक विन्यास लिखिए।
उत्तर
प्रथम संक्रमण श्रेणी में उपस्थित तत्वों के नाम, संकेत तथा इलेक्ट्रॉनिक विन्यास –
प्रश्न 20.
f-ब्लॉक तत्वों का सामान्य इलेक्ट्रॉनिक विन्यास लिखिए। लैन्थेमाइड्स के कोई दो उपयोग लिखिए। ऐक्टिनाइड्स के कोई तीन उपयोग लिखिए।
उत्तर
ब्लॉक तत्वों का सामान्य विन्यास –
(n-2)f1-14, (n-1) s2p6 d0-1,ns2 होता है।
लैन्थेनाइड्स के दो उपयोग –
(i) ज्वलनशील मिश्रधातु बनाने में
(ii) धूप के चश्मों में
(iii) रंगीन काँच व फिल्टर बनाने में।
ऐक्टिनाइड्स के उपयोग –
(i) नाभिकीय रिएक्टर में
(ii) कैंसर के उपचार में थोरियम का उपयोग
(iii) प्लूटोनियम का उपयोग परमाणु बम, परमाणु भट्ठी में होता है।
प्रश्न 21.
K2Cr2O7 एवं KMnO4 के उपयोग बताइए। .
उत्तर
K2Cr2O7 के उपयोग- (i) ऑक्सीकारक के रूप में, (ii) रंगाई व छपाई में, (iii) आयतनमितीय विश्लेषण में, (iv) क्रोमेटेजिंग में।
KMnO4 के उपयोग-(i) ऑक्सीकारक के रूप में, (ii) आयतनात्मक विश्लेषण में, (iii) कार्बनिक यौगिकों के निर्माण में, (iv) संक्रमणरोधी के रूप में।
प्रश्न 22.
अप्रारूपी संक्रमण तत्व एवं प्रारूपी संक्रमण तत्व किसे कहते हैं ?
उत्तर
Zn, Cd तथा Hg के परमाणुओं में (n-1)d उपकक्ष पूर्ण होते है। अत: इन तत्वों को d- समुदाय तत्व नहीं मानना चाहिए। इसी प्रकार ये तत्व d- समुदाय के तत्वों से गुणों के आधार पर बहुत कम समानता रखते हैं। परन्तु फिर भी ये तत्व d- समुदाय के तत्व कहलाते हैं । अत: Zn, Cd तथा Hg को अप्रारूपी संक्रमण तत्व कहा जाता है। जबकि अन्य संक्रमण तत्वों को प्रारूपी संक्रमण तत्व कहा जाता है।
प्रश्न 23.
Cu+ रंगहीन है परन्तु Cu2+ रंगीन होता है, क्यों?
उत्तर
Cu+ का उपकोश पूर्ण भरा होता है। इस प्रकार इनका d – d संक्रमण नहीं होता और वह सफेद अथवा रंगहीन रहता है। जबकि Cu2+ में अयुग्मित 3d इलेक्ट्रॉन होने के कारण एवं d-d संक्रमण सम्भव होने के कारण वह रंगीन होता है।
प्रश्न 24.
संक्रमण तत्व क्या है ? इन्हें कितनी श्रेणियों में विभाजित किया गया है ?
उत्तर
वे तत्व जिनमें परमाण्विक अवस्था में d-कक्षक आंशिक रूप से भरे हुए हों, संक्रमण तत्व कहलाते हैं, इन्हें 4 श्रेणियों में वर्गीकृत किया जा सकता है –
1. प्रथम संक्रमण श्रेणी (3d- Series)- इसमें चतुर्थ आवर्त के Sc21 स्कैंडियम से जिंक (Zn = 30) तक 10 तत्व हैं।
2. द्वितीय संक्रमण श्रेणी (4d- Series)- इसमें पंचम आवर्त के इट्रियम Y39 से कैडमियम Cd48 तक 10 तत्व हैं।
3. तृतीय संक्रमण श्रेणी (5d- Series)- इसमें छठे आवर्त के लैन्थेनम (La = 57) तथा (Hf =72) से मर्करी (Hg = 80) तक के 10 तत्व हैं।
4. चतुर्थ संक्रमण श्रेणी(6d- Series)- इसमें सातवें आवर्त ऐक्टीनियम (Ac=89) तथा रदरफोर्डियम (Rf =72) तथा हाड्रियम (Ha = 105) हैं ये श्रेणी अभी अपूर्ण है।
प्रश्न 25.
संक्षेप में स्पष्ट कीजिए कि प्रथम संक्रमण श्रेणी के प्रथम अर्द्धभाग में बढ़ते हुए परमाणु क्रमांक के साथ +2 ऑक्सीकरण अवस्था कैसे अधिक स्थायी होती जाती है?
उत्तर
(IE1 + IE2) आयनन ऊर्जा का मान बढ़ता है। परिमाणस्वरुप मानक अपचयन विभव E0 कम होता जाता है। अत: M+2 आयन बनने की क्षमता घटती है। Mn+2 के लिए उच्च क्षमता अर्द्धपूर्ण इलेक्ट्रॉनिक विन्यास के कारण है। इसलिए प्रथम सदस्य के लिए इलेक्ट्रॉनिक विन्यास 3d14s2 है, जिनमें तीन इलेक्ट्रॉन दान करने की क्षमता होती है। अतः +2 ऑक्सीकरण अवस्था की तुलना में +3 ऑक्सीकरण अवस्था की प्रबलता अधिक है।
d एवं f-ब्लॉक के तत्त्व दीर्घ उत्तरीय प्रश्न
प्रश्न 1.
लैन्थेनाइड का इलेक्ट्रॉनिक विन्यास देते हुए इसके ऑक्सीकरण अवस्था को समझाइए।
उत्तर
अन्तर संक्रमण तत्त्वों की दो श्रेणियों में एक है लैन्थेनाइड या 4fश्रेणी । इस श्रेणी के तत्त्वों में 4fकक्षक में क्रमशः इलेक्ट्रॉन भरते हैं । इनका सामान्य इलेक्ट्रॉनिक विन्यास [Xe] 4f1-145d1-26s2 होता है। इनकी कुल संख्या 14 है जो सीरियम (परमाणु क्रमांक 58) से प्रारम्भ होकर ल्यूटीशियम (परमाणु क्रमांक 71) पर समाप्त होती है ।
ऑक्सीकरण अवस्था – लैन्थेनाइड तत्त्वों की सर्वाधिक ऑक्सीकरण अवस्था (+3) होती है। यह लैन्थेनम से दो और एक d-कक्षक के इलेक्ट्रॉन के खोने से बनती है। La3+ का विन्यास जेनॉन (Xe = 54) जैसा होता है जो कि अत्यधिक स्थायी होता है। कुछ तत्व (+ 2) और (+4) ऑक्सीकरण भी प्रदर्शित करते हैं क्योंकि ये तत्व 2 या 4 इलेक्ट्रॉन खोने के बाद स्थायी f7 या f14 विन्यास प्राप्त करते हैं।
उदाहरणार्थ – Ce4+(4f°), Tb+ (4f7),Eu2+ (4f7), Yb2+ (4f14), परन्तु Sm2+, Tm2+ इसके अपवाद हैं।
सामान्यतः लैन्थेनाइड में +4 ऑक्सीकरण अवस्था प्रबल ऑक्सीकरण का कार्य करती है, जैसे Ce+4 आयन जलीय विलयन का अच्छा ऑक्सीकरक है जो +4 से +3 में परिवर्तित हो जाता है तथा दूसरी ओर लैन्थेनाइड में +2 ऑक्सीकरण अवस्था प्रबल अपचायक की तरह कार्य करती है। जैसे-Sm+2, Eu+2 और Yb+2 आयन अच्छा अपचायक है जो जलीय विलयन में +2 से +3 में ऑक्सीकृत हो जाता है।
प्रश्न 2.
क्रोमाइट अयस्क से K2Cr2O7 बनाने की विधि लिखिए तथा K2Cr2O7 की अम्लीय FeSO4 KI एवं H2S के मध्य अभिक्रिया के लिए संतुलित समीकरण लिखिए।
उत्तर
बनाने की विधि-K2Cr2O7 को क्रोमाइट अयस्क (Fe2Cr2O4) या क्रोम आयरन (FeO.Cr203) से बनाया जाता है, जो निम्नलिखित पदों में होते हैं।
(1) क्रोमाइट अयस्क का सोडियम क्रोमेट में परिवर्तन-क्रोमाइट अयस्क को NaOH या Na2CO3 के साथ वायु की उपस्थिति में एक परावर्तनी भट्टी में गर्म करने पर सोडियम क्रोमेट (पीला रंग) बनता है।
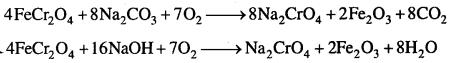
पदार्थ को छिद्रमय रखने हेतु कुछ मात्रा में शुष्क चूने को मिलाते हैं । जल के साथ निष्कर्षण करने पर Na2Cr2O3 विलयन में चला जाता है। जबकि Fe2O3 रह जाता है जिसे छानकर पृथक् कर लेते हैं।
(2) सोडियम क्रोमेट (Na2CrO4) का सोडियम डाइक्रोमेट (Na2Cr2O7) में परिवर्तन-सोडियम क्रोमेट विलयन सान्द्र H2SO4 के साथ अपचयित करके सोडियम डाइक्रोमेट बनाते हैं।
![]()
2Na2CrO4 कम विलेय होता है जिसका वाष्पन करने पर Na2SO410H2O के रूप में क्रिस्टलीकृत हो जाता है जिसे पृथक् कर लिया जाता है।
(3) Na2Cr2O7 का K2Cr2O7 में परिवर्तन-सोडियम डाइक्रोमेट के जलीय विलयन का उपचार KCI के साथ किये जाने पर पोटैशियम डाइ क्रोमेट प्राप्त होता है। K2Cr207 के अल्प विलेय प्रकृति के कारण इसके क्रिस्टल ठण्डे में प्राप्त किये जाते हैं।
![]()
K2Cr2O7 की निम्न के साथ होने वाली रासायनिक अभिक्रिया –
(1) अम्लीय फेरस सल्फेट के साथ-K2Cr207 अम्लीय माध्यम में यह फेरस सल्फेट को फेरिक सल्फेट में ऑक्सीकृत कर देता है। K2Cr2O7 पहले H2SO4 से क्रिया करके नवजात ऑक्सीजन का तीन परमाणु देता है जो Fe2+ को Fe3+ आयन में ऑक्सीकृत कर देता है।

प्रश्न 3.
अम्लीय, क्षारीय तथा उदासीन माध्यम में KMnO के ऑक्सीकारक गुण को दो-दो उदाहरण द्वारा समझाइए।
अथवा, पोटैशियम परमैंगनेट के अम्लीय माध्यम में कोई ऑक्सीकारक गुणों को समीकरण द्वारा समझाइए।
उत्तर
KMnO4 का विलयन उदासीन हो, क्षारीय हो या अम्लीय हो, प्रत्येक परिस्थिति में यह तीव्र ऑक्सीकारक का कार्य करता है।
(1) अम्लीय माध्यम में-तनु H2SO4 की उपस्थिति में KMnO4 अपचयित हो जाता है तथा इसके दो अणुओं से ऑक्सीजन के पाँच परमाणु प्राप्त होते हैं।
2KMnO4 + 3H2SO4→K2SO4 + 2MnSO4 + 3H2O + 5[0]
उदाहरण – (i) फेरस लवण का फेरिक लवण में ऑक्सीकरण –
अम्लीय KMnO4 से प्राप्त नवजात ऑक्सीजन फेरस लवण को फेरिक लवण में ऑक्सीकृत करता है।
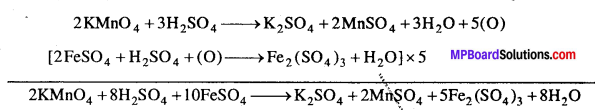
(ii) ऑक्जेलिक अम्ल का ऑक्सीकरण-अम्लीय माध्यम में KMnO4 ऑक्जेलिक अम्ल को CO2 में ऑक्सीकृत कर देता है।
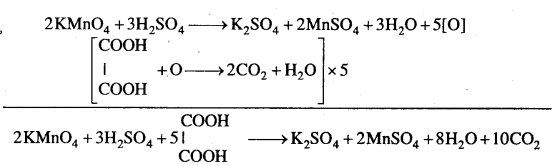
(iii) आयोडाइड आयन का आयोडीन में परिवर्तन
![]()
(iv) नाइट्राइट का नाइट्रेट में ऑक्सीकरण
![]()
(2) क्षारीय माध्यम में-क्षारीय माध्यम में KMnOa, MnO, में अपचयित होता है तथा 3 नवजात ऑक्सीजन देता है।
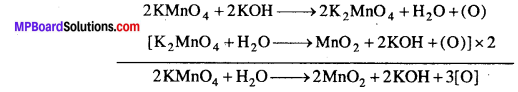
उदाहरण-(i) आयोडाइड का आयोडेट में ऑक्सीकरणक्षारीय माध्यम में KI का आयोडेट में ऑक्सीकरण होता है।
2KMnO4 + H2O +KI→KIO3 +2MnO2 + 2KOH
(ii) एथिलीन का ग्लाइकॉल में ऑक्सीकरण –
क्षारीय KMnO4 एथिलीन का एथिलीन ग्लाइकॉल में ऑक्सीकरण करता है।

(3) उदासीन माध्यम में-उदासीन माध्यम में भी KMnO4 ऑक्सीकारक की तरह कार्य करता है। अभिक्रिया में बना KOH विलयन को क्षारीय बना देता है। KMnO4, MnO2 में अपचयित हो जाता है एवं 2 मोल KMnO4 से 2 मोल नवजात ऑक्सीजन मुक्त होते हैं।

प्रश्न 4.
पायरोलुसाइट से KMnO4 बनाने की विधि लिखिए तथा KMnO4 की अम्लीय, क्षारीय तथा उदासीन माध्यम में ऑक्सीकारक गुणों को एक-एक उदाहरण देकर समझाइए।
उत्तर
पायरोलुसाइट से KMnO4 का निर्माण
1. पायरोलुसाइट का KMnO4 (हरे पदार्थ) में परिवर्तन-पायरोलुसाइट को वायुमण्डलीय O2 में KOH या K2CO3 के साथ गलित करने पर पोटैशियम मैंगनेट का हरा पदार्थ बनता है।
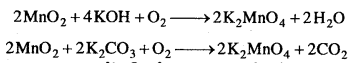
2. K2MnO4 का KMnO4 में परिवर्तन-K2MnO4 के हरे पदार्थ को जल के साथ निष्कासित करके रासायनिक ऑक्सीकरण या विद्युत्-अपघटनी ऑक्सीकरण द्वारा KMnO4 में ऑक्सीकृत करते हैं।
(a) रासायनिक ऑक्सीकरण-KMnO4 के हरे विलयन का उपचार Cl2, O2 या CO2 की धारा में प्रवाहित करके KMnO में ऑक्सीकृत किया गया है।
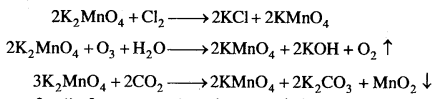
(b) विद्युत्-अपघटनी ऑक्सीकरण-इस विधि में आयरन कैथोड एवं निकिल ऐनोड के मध्य K2MnO4 विलयन का विद्युत्-अपघटन किया जाता है, तो मैंगनेट आयन का ऐनोड पर परमैंगनेट आयन (MnO–4) में ऑक्सीकरण हो जाता है तथा कैथोड पर H, मुक्त होती है।
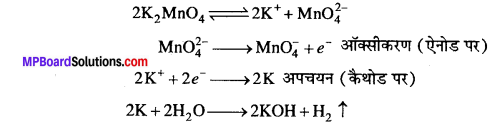
अम्लीय, क्षारीय तथा उदासीन माध्यम में ऑक्सीकारक गुणों के उदाहरण-दीर्घ उत्तरीय प्रश्न क्र. 3 देखिए।