MP Board Class 11th Chemistry Solutions Chapter 4 रासायनिक आबंधन तथा आण्विक संरचना
रासायनिक आबंधन तथा आण्विक संरचना NCERT अभ्यास प्रश्न
प्रश्न 1.
रासायनिक आबंध के बनने की व्याख्या कीजिए।
उत्तर:
समान और भिन्न तत्वों के परमाणु आपस में मिलकर रासायनिक आबंध बनाते हैं। इस प्रकार बने रासायनिक आबंधों को विभिन्न सिद्धांतों द्वारा वर्णित किया गया है। जब समान या भिन्न तत्वों के परमाणु संयोग करते हैं तब वे अपने संयोजी कोश में अष्टक पूरा करते हैं। अष्टक पूरा करके तत्व आदर्श गैस के विन्यास को ग्रहण करते हैं। ऐसे परमाणु या तो इलेक्ट्रॉन का साझा करके या दान करके करते हैं। एक अन्य सिद्धांत के अनुसार जब परमाणु आबंध बनाते हैं तब प्रक्रम का ऊर्जा स्तर निम्नतम होता है जिससे स्थायित्व ग्रहण करते हैं।
प्रश्न 2.
निम्नलिखित तत्वों के परमाणुओं के लुईस बिंदु प्रतीक लिखिए –
Mg, Na, B, O, N, Br.
उत्तर:
![]()
प्रश्न 3.
निम्नलिखित परमाणुओं तथा आयनों के लुईस बिन्दु प्रतीक लिखिए –
P और P3-, Na और Na+, S और S2-, Al और Al3+, H और H.
उत्तर:
![]()
प्रश्न 4.
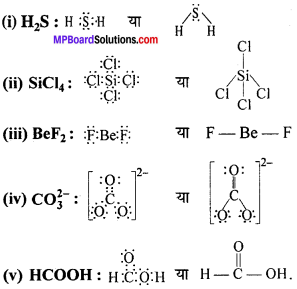
निम्नलिखित अणुओं तथा आयनों की लुईस संरचनाएँ लिखिए –
H2S, SiCl4, BeF4, CO32-, HCOOH.
उत्तर:
प्रश्न 5.
अष्टक नियम को परिभाषित कीजिए तथा इस नियम के महत्व और सीमाओं को लिखिए।
उत्तर:
अष्टक नियम-इस नियम का प्रतिपादन लुईस ने किया था। उनके अनुसार यदि किसी तत्व के संयोजी कोश में आठ इलेक्ट्रॉन हैं तब तत्व रासायनिक रूप से निष्क्रिय होता है। लेकिन यदि बाहरी कोश में इलेक्ट्रॉन न हों तो परमाणु या अणु का निर्माण करते समय इलेक्ट्रॉन का आदान-प्रदान या साझा करके आठ इलेक्ट्रॉन पूर्ण करने का प्रयास करता है, यही अष्टक नियम कहलाता है।
उदाहरण:
SF6, PCl5, तथा IF7, जैसे यौगिकों के संयोजी कोश में 12, 10 तथा 14 इलेक्ट्रॉन हैं। दूसरी ओर BF3, तथा BeCl2 के संयोजी कोश में क्रमशः 6 तथा 4 इलेक्ट्रॉन हैं।
आवर्त सारणी के दूसरे तत्व जो संयोजी कक्षा में आठ से कम इलेक्ट्रॉन रखते हैं रासायनिक सक्रिय है। अतः जिनके संयोजी इलेक्ट्रॉन आठ से कम होते हैं सक्रिय होते हैं।
अष्टक नियम की सीमाएँ
- केन्द्रीय परमाणु का अपूर्ण अष्टक – कुछ यौगिकों में केन्द्रीय परमाणु के चारों ओर उपस्थित इलेक्ट्रॉनों की संख्या आठ से कम होती है। जैसे-H : H, Li : Cl, H : Be : H.
- विषम इलेक्ट्रॉन अणु – उन अणुओं जिनमें इलेक्ट्रॉनों की कुल संख्या विषम होती है ये सभी परमाणु अष्टक नियम का पालन नहीं कर पाते।
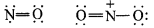
- प्रसारित अष्टक – इन तत्वों के अनेक यौगिकों में केन्द्रीय परमाणु के चारों ओर आठ से अधिक इलेक्ट्रॉन होते हैं इसे प्रसारित अष्टक कहते हैं।

- उदासीन परमाणु से संबंधित धनायनों एवं ऋणायनों के बनने की सरलता।
- धनायनों एवं ऋणायनों को ठोस में व्यवस्थित होने की विधि अर्थात् क्रिस्टलीय यौगिक का जालक निर्मित होने की विधि।
प्रश्न 6.
आयनिक आबंध बनाने के लिए अनुकूल कारकों को लिखिए।
उत्तर:
आयनिक आबंध बनाने हेतु अनुकूल कारक निम्न हैं –
- धनायन बनाने वाले तत्व का आयनन विभव निम्न होना चाहिए।
- ऋणायन बनाने वाले तत्व की उच्च इलेक्ट्रॉन ग्रहण एन्थैल्पी।
- आयनिक यौगिक की उच्च जालक ऊर्जा होना।
प्रश्न 7.
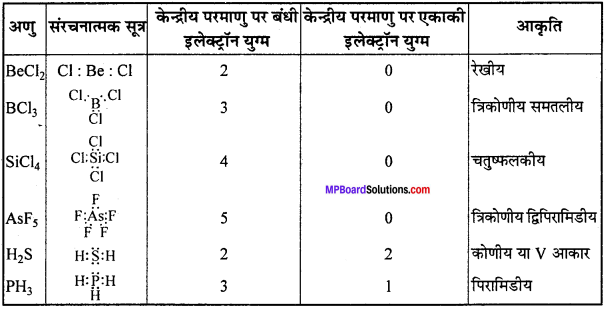
निम्नलिखित अणुओं की आकृति की व्याख्या वी.एस.ई.पी.आर. सिद्धान्त के अनुरूप कीजिए –
BeCl2, BCl3, SiCl4, AsF5, H2S, PH3.
उत्तर:
सहसंयोजक अणुओं की आकृति VSEPR सिद्धान्त के अनुसार निम्नानुसार होगी –
प्रश्न 8.
यद्यपि NH3 तथा H2O दोनों अणुओं की ज्यामिति विकृत चतुष्फलकीय होती है, तथापि जल में आबंध कोण अमोनिया की अपेक्षा कम होता है। विवेचना कीजिए।
उत्तर:
H2O के अणु में 2 एकाकी इलेक्ट्रॉन युग्म एवं NH3 में 1 एकाकी इलेक्ट्रॉन युग्म होता है। VSEPR सिद्धान्त के अनुसार दो एकक इलेक्ट्रॉन युग्मों में ज्यादा प्रतिकर्षण होता है जिससे बंध कोण का मान कम हो जाता है अत: H2O में बन्ध कोण 104.5° तथा NH3 में 107° का होता है।
प्रश्न 9.
आबंध प्रबलता को आबंध-कोटि के रूप में आप किस प्रकार व्यक्त करेंगे? उत्तर-आबंध कोटि बढ़ने पर आबंध प्रबलता का मान भी बढ़ता है। प्रश्न 10. आबंध लंबाई की परिभाषा दीजिए।
उत्तर:
किसी अणु की बंध लम्बाई अणु में आबंधित परमाणुओं के नाभिकों के मध्य साम्यावस्था पर दूरी का मान होता है।
प्रश्न 11.
Coआयन के संदर्भ में अनुनाद के विभिन्न पहलुओं को स्पष्ट कीजिए।
उत्तर:
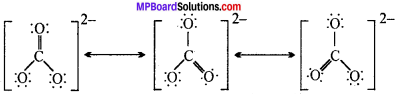
कार्बन तथा ऑक्सीजन परमाणुओं के मध्य दो एकल आबंध तथा एक द्वि-आबंध वाली लुईस संरचना कार्बोनेट आयन की वास्तविक संरचना को निरूपित करने के लिए अपर्याप्त है क्योंकि इसके अनुसार तीन कार्बन-ऑक्सीजन आबंधों की लम्बाई भिन्न-भिन्न होनी चाहिए।
कार्बोनेट आयन (CO32-) – 24 इलेक्ट्रॉन निकाय (अनुनादी संरचनाएँ) –
प्रश्न 12.
नीचे दी गई संरचनाओं (1 तथा 2) द्वारा H3PO3 को प्रदर्शित किया जा सकता है। क्या ये दो संरचनाएँ H3PO3 के अनुनाद संकर के विहित (कैनोनिकल) रूप माने जा सकते हैं? यदि नहीं, तो उसका कारण बताइए।

उत्तर:
नहीं, H3PO3 की दी गई संरचनाएँ अनुनादी संकर के विहित (कैनोनिकल) रूप नहीं माने जा सकते क्योंकि इन संरचनाओं में परमाणुओं के स्थान परिवर्तित हो रहे हैं।
प्रश्न 13.
SO3, NO2, तथा NO3– की अनुनादी संरचनाएँ लिखिए।
उत्तर:
1. SO3 की अनुनादी संरचनाएँ –
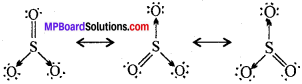
2. NO2 की अनुनादी संरचनाएँ –
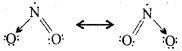
3. NO3– की अनुनादी संरचनाएँ –
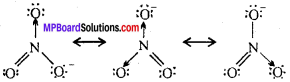
प्रश्न 14.
निम्नलिखित परमाणुओं से इलेक्ट्रॉन स्थानांतरण द्वारा धनायनों तथा ऋणायनों में विरचन को लुईस बिन्दु-प्रतीकों की सहायता से दर्शाइए
(a) K तथा S
(b) Ca तथा O
(c) Al तथा N.
उत्तर:
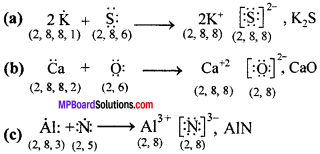
प्रश्न 15.
हालाँकि CO2 तथा H2O दोनों त्रिपरमाणुक अणु है, परंतु H2O अणु की आकृति बंकित होती है, जबकि CO2 की रैखिक आकृति होती है। द्विध्रुव आघूर्ण के आधार पर इसकी व्याख्या कीजिए।
उत्तर:
CO2 की संरचना रैखिक होने के कारण CO2 में दो समान बंध आघूर्ण विपरीत दिशा में कार्य करते हैं और एक-दूसरे के प्रभाव को समाप्त कर देते हैं।
![]()
जबकि H2O की कोणीय (मुड़ी हुई) संरचना के कारण O-H के द्विध्रुव एक-दूसरे को उदासीन या निष्क्रिय नहीं कर पाते हैं।
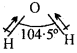
प्रश्न 16.
द्विध्रुव आघूर्ण के महत्वपूर्ण अनुप्रयोग बताइए।
उत्तर:
द्विध्रुव आघूर्ण के महत्वपूर्ण अनुप्रयोग निम्नलिखित हैं –
1. आबंध की घूर्णता ज्ञात करने में:
जैसा कि µ = e x d का मान जितना अधिक होगा द्विध्रुव आघूर्ण का मान उतना ही ज्यादा होगा, यह एकल घूर्णन आबंध पर लागू होता है। जैसे – HCl, HBr आदि। आघूर्ण अणु जैसे H2, O2, N2, आदि की द्विध्रुव घूर्णता शून्य होता है। क्योंकि इन अणुओं में आवेश विभाजित नहीं होता है। अतः द्विध्रुव आघूर्ण, ध्रुवीय व अध्रुवीय अणुओं में अन्तर बताता है।
2. आयनिक प्रतिशतता ज्ञात करने में:
उदाहरण – HCl में = 1.03D यदि HCl 100% आयनित है तब प्रत्येक इकाई पर एक इकाई आवेश होगा अर्थात् 4.8 x 10-10-10 + 5.4 आबंध दूरी (H-Cl) = 1.275 Å
∴ 100% आयनन गुणधर्म के लिए
= 4.8 x 10-10 x 1.275 x 10-8
= 6.12 x 10-18 e.s.u. = 6.12D
% आयनन = \(\frac{1.03}{6.12}\) x 100 = 1686.
3. अणुओं की आकृति ज्ञात करने में:
अणुओं की आकृति ज्ञात करने में द्विध्रुव आघूर्ण महत्वपूर्ण गुणधर्म होता है। ऐसा अणु जिसमें तीन या अधिक परमाणु होते हैं, के लिए द्विध्रुव आघूर्ण महत्वपूर्ण है। यदि किसी अणु में एक या अधिक ध्रुव आबंध होते हैं और वह रेखीय नहीं है यदि एक द्विध्रुव आघूर्ण होता है जैसा कि जल के अणु H2O के लिए µ = 1.84D है और अमोनिया µ = 1.49D होता है के लिए आकृति बंकित होती है जिन अणुओं में µ = 0 होता है वे अणु रेखीय आकृति के होते हैं। जैसे – CO2, BF3, CH4 या CCl4 आदि।
प्रश्न 17.
विद्युत्-ऋणात्मकता को परिभाषित कीजिए। यह इलेक्ट्रॉन ग्रहण एन्थैल्पी से किस प्रकार भिन्न है?
उत्तर:
सहसंयोजी आबंध में किसी परमाणु की वह क्षमता जिसके कारण आबंधी इलेक्ट्रॉन को अपनी ओर आकर्षित करता है, विद्युत्-ऋणात्मकता कहलाती है। विद्युत्-ऋणात्मकता अणु में परमाणु के इस गुण धर्म को दर्शाती है, जबकि इलेक्ट्रॉन ग्रहण एन्थैल्पी एकल परमाणु के गुणधर्म को दर्शाता है।
इलेक्ट्रॉन ग्रहण एन्थैल्पी:
- इलेक्ट्रॉन ग्रहण एन्थैल्पी एक परिमाणात्मक मान है एवं उस ऊर्जा को व्यक्त करती है, जो एक विलगित गैसीयपरमाणु के अंतिम कक्ष में एक इलेक्ट्रॉन को प्रविष्ट कराने पर मुक्त होती है।
- ये विलगित अणु का गुण है।
- एक अणु की इलेक्ट्रॉन ग्रहण एन्थैल्पी का निरपेक्ष मान होता है।
- परिमाणात्मक होने के कारण इसका मात्रक होता है एवं इसे eV प्रति परमाणु या kJ प्रति मोल में व्यक्त करते हैं।
विद्युत्-ऋणात्मकता:
- विद्युत्-ऋणात्मकता सहसंयोजी आबंधी इलेक्ट्रॉन युग्म को परमाणु द्वारा अपनी ओर आकर्षित करने की प्रवृत्ति होती है।
- ये बंधित अणु का गुण है।
- विद्युत्-ऋणात्मकता का मान बंध पर निर्भर करता है।
- यह तत्वों के बीच आपेक्षिक होती है इसलिए इसकी कोई इकाई नहीं होती।
प्रश्न 18.
ध्रुवीय सहसंयोजी आबंध से आप क्या समझते हैं? उदाहरण सहित व्याख्या कीजिए।
उत्तर:
दो असमान परमाणुओं के मध्य बनने वाला सहसंयोजी बंध में इनके विद्युत्-ऋणात्मकता में अन्तर के कारण ध्रुवीय गुण होता है क्योंकि आबंधित इलेक्ट्रॉन युग्म अधिक विद्युत्-ऋणात्मक परमाणु की ओर विस्थापित हो जाता है। ऐसा बंध ध्रुवीय सहसंयोजी बंध कहलाता है।
उदाहरणार्थ –
![]()
आबंधी इलेक्ट्रॉन बंध का F परमाणु की ओर आकर्षित होना ध्रुवीय सहसंयोजी बंध का निर्माण करना है।
प्रश्न 19.
निम्नलिखित अणुओं को आबंधों की बढ़ती आयनिक प्रकृति के क्रम में लिखिए –
LiF, K2O, N2, SO2, तथा CIF3.
उत्तर:
N2 < SO2 < CIF3 < K2O < LiF.
प्रश्न 20.
CH3COOH की नीचे दी गई ढाँचा-संरचना सही है, परंतु कुछ आबंध त्रुटिपूर्ण दर्शाए गए हैं। ऐसीटिक अम्ल की सही लुईस-संरचना लिखिए –
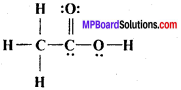
उत्तर:
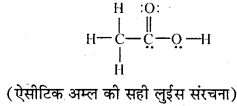
प्रश्न 21.
चतुष्फलकीय ज्यामिति के अलावा CH4 अणु की एक और संभव ज्यामिति वर्गसमतलीय है, जिसमें हाइड्रोजन के चार परमाणु एक वर्ग के चारों कोनों पर होते हैं। व्याख्या कीजिए कि CH4 का अणु वर्ग-समतलीय नहीं होता है।
उत्तर:
वर्ग समतलीय ज्यामिति में बंध कोण 90° का होता है जिसमें चतुष्फलकीय ज्यामिति बंध कोण 109°28′ की तुलना में अधिक प्रतिकर्षण (कम स्थायित्व) होता है। अत: अधिक स्थाई अवस्था (कम प्रतिकर्षण)वाली अवस्था चतुष्फलकीय ज्यामिति ही CH4 की वास्तविक अवस्था होगी।
प्रश्न 22.
यद्यपि Be-H आबंध ध्रुवीय है, तथापि BeH2 अणु का द्विधुव आघूर्ण शून्य है। स्पष्ट कीजिए।
उत्तर:
चूँकि BeH2, अणु की संरचना रेखीय होती है अतः इसके दो Be – H आबंध एक-दूसरे के प्रभाव को समाप्त कर देते हैं एवं BeH2 का द्विध्रुव आघूर्ण शून्य होता है।
![]()
प्रश्न 23.
NH3 तथा NF3 में किस अणु का द्विध्रुव-आघूर्ण अधिक है और क्यों?
उत्तर:
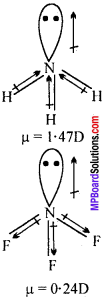
NH2 तथा NF3 के द्विध्रुव आघूर्ण की तुलना-इन दोनों में नाइट्रोजन में एक एकाकी युग्म के कारण इनका आकार पिरामिडीय होता है। फ्लुओरीन की विद्युत्ऋणात्मकता हाइड्रोजन से अधिक होने के कारण N – F बंध, N – H बंध की तुलना में अधिक ध्रुवीय होता है अत: NF3 का परिणामी द्विध्रुव आघूर्ण NH3 से अधिक होनी चाहिए परन्तु NH4 का द्विध्रुव आघूर्ण (µ = 1.47D), NF3 (µ = 0.24D) से अधिक होता है। इस असामान्य व्यवहार को नाइट्रोजन पर उपस्थित एकाकी इलेक्ट्रॉन युग्म द्वारा समझा जा सकता है। NH3 में एकाकी इलेक्ट्रॉन युग्म के कारण कक्षीय द्विध्रुव तथा तीन N – H बंध का बंध आघूर्ण एक ही दिशा में होता है। अतः परिणामी द्विध्रुव आघूर्ण N – H बंध में जुड़ते हैं जबकि NF3 में कक्षीय द्विध्रुव आघूर्ण की दिशा तीन N – F बंध के परिणामी द्विध्रुव आघूर्ण के विपरीत होती है। अतः एकाकी युग्म का आघूर्ण परिणामी N – F बंध आघूर्ण को चित्र में दिखाये अनुसार निरस्त कर देते हैं। अत: NF3 का द्विध्रुव आघूर्ण कम होता है।
प्रश्न 24.
परमाणु-कक्षकों के संकरण से आप क्या समझते हैं? sp, sp2 तथा sp3 संकर कक्षकों की आकृति का वर्णन कीजिए।
उत्तर:
संकरण:
परमाणु कक्षक संयोजित होकर समतुल्य कक्षकों का समूह बनाते हैं। इन कक्षकों को संकर कक्षक कहते हैं। आबंध विचरन में परमाणु शुद्ध कक्षकों के स्थान पर संकरित कक्षकों का प्रयोग करते हैं। इस परिघटना को संकरण कहते हैं। लगभग समान ऊर्जा वाले कक्षकों के आपस में मिलकर ऊर्जा के पुनर्वितरण द्वारा समान ऊर्जा तथा आकार वाले कक्षकों को बनाने की प्रक्रिया को संकरण कहते हैं।
1. sp संकरण – इस प्रकार के संकरण में एक s तथा एक p कक्षक संकरित होकर दो समान sp संकरण कक्षकों का निर्माण करते हैं।
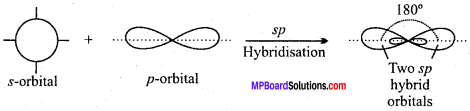
2. sp2संकरण – इस प्रकार के संकरण में एक s तथा दो p कक्षक संकरित होकर तीन समान sp संकर कक्षकों का निर्माण करते हैं।
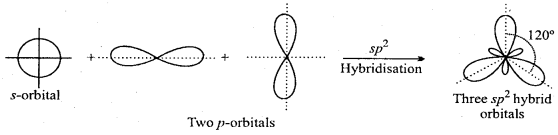
3. sp3 संकरण – इस संकरण में एक ऽ तथा तीन p कक्षक संकरित होकर चार समान sp’ संकर कक्षकों का निर्माण करते हैं।
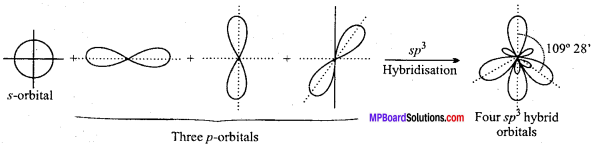
प्रश्न 25.
निम्नलिखित अभिक्रिया में AI परमाणु की संकरण अवस्था में परिवर्तन (यदि होता है, तो) को समझाइए –
AlCl3 + Cl– → AlCl4–
उत्तर:
AlCl3 में Al, sp2 संकरित अवस्था में है जबकि [AlCl4]– में Al, sp3 संकरित होता है।
प्रश्न 26.
क्या निम्नलिखित अभिक्रिया के फलस्वरूप B तथा N परमाणुओं की संकरण अवस्था में परिवर्तन होता है
BF3 + NH3 → F3B.NH3
उत्तर:
उपर्युक्त अभिक्रिया में N का संकरण अपरिवर्तित रहता है जबकि B का संकरण sp2 से sp3 हो जाता है।
प्रश्न 27.
C2H4, तथा C2H2, अणुओं में कार्बन परमाणुओं के बीच क्रमशः द्वि-आबंध तथा त्रिआबंध के निर्माण को चित्र द्वारा स्पष्ट कीजिए।
उत्तर:
ऐथीन (एथिलीन, C2H4) अणु:
संकरित कार्बन परमाणु के एक s कक्षक तथा दो p कक्षक मिश्रित होकर तीन sp2 संकरित कक्षकों का निर्माण करते हैं। तीसरा p कक्षक, जो संकरण में भाग नहीं लेता, एक अक्ष की दिशा में ही स्थित रहता है तथा उसी स्थिति में बंध बनाता है। तीन sp2संकरित कक्षक एक समत्रिभुज के तीन शीर्षों की ओर इंगित करते हुए होते हैं। पहले कार्बन परमाणु का एक sp कक्षक दूसरे कार्बन परमाणु के एक sp कक्षक से अक्षीय अतिव्यापन (Axial overlapping) करके C – C बंध बनाता है। प्रत्येक कार्बन पर स्थित शेष दो sp2 कक्षक जो 120° का कोण बनाते हैं, हाइड्रोजन के 1s कक्षक के साथ अतिव्यापन करके C – H बन्ध बनाते हैं। इस प्रकार कुल चार C – H बन्ध बनते हैं। इसके अतिरिक्त प्रत्येक कार्बन परमाणु पर एक-एक असंकरित p कक्षक हैं जो पार्श्व अतिव्यापन करके दूसरा C – C बन्ध बनाते हैं। इस प्रकार C2H4 बनता है जिसमें कार्बन परमाणुओं के मध्य द्विबन्ध (Double bond) होता है। sp2 संकरण से C2H4, अणु का बनना चित्र में दर्शाया गया है।
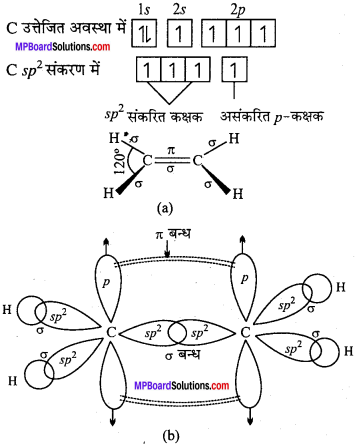
एसीटिलीन (C2H2) अणु:
C2H2, अणु में sp संकरण होता है। एथाइन अणु के बनने में दोनों कार्बन परमाणु sp संकरण दर्शाते हैं। उन पर दो-दो संकरित (2p, तथा 2p.) कक्षक होते हैं। एक कार्बन परमाणु का sp संकर कक्षक दूसरे कार्बन परमाणु के sp संकर कक्षक से अक्षीय अतिव्यापन द्वारा C – C सिग्मा आबंध बनाता है। बचे हुए संकर कक्षक हाइड्रोजन के अर्धवृत्त 1s कक्षकों से अक्षीय अतिव्यापन द्वारा सिग्मा आबंध बनाते हैं दोनों कार्बन परमाणुओं पर उपस्थित दो-दो असंकरित कक्षक पार्श्व अतिव्यापन द्वारा दो पाई-आबंध बनाता है।

प्रश्न 28.
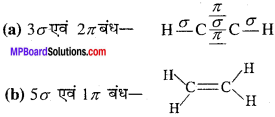
निम्नलिखित अणुओं में सिग्मा (σ) तथा पाई (π) आबंधों की कुल संख्या कितनी है –
(a) C2H2
(b) C2H4
उत्तर:
प्रश्न 29.
X-अक्ष को अंतर्नाभिकीय अक्ष मानते हुए बताइए कि निम्नलिखित में कौन-से कक्षक सिग्मा (σ) आबंध नहीं बनाएँगे और क्यों –
(a) 1s तथा 1s
(b) 15 तथा 2px
(c) 2py तथा 2py
(d) 1s तथा 2s.
उत्तर:
(c) को छोड़कर सभी बन्ध बनाएँगे, चूँकि 2p,-2p, के मध्य पार्श्व अतिव्यापन होगा जिससे गबन्ध बनेगा।
प्रश्न 30.
निम्नलिखित अणुओं में कार्बन परमाणु कौन-से संकर कक्षक प्रयुक्त करते हैं –
(a) CH3 – CH3
(b) CH3 – CH = CH2
(c) CH3 – CH2 – OH
(d) CH3CHO
(e) CH3COOH
उत्तर:
(a) sp3 – sp3
(b) sp3 – sp2 – sp3
(c) sp3 – sp3
(d) sp2 – sp2
(e) sp3 – sp2
प्रश्न 31.
इलेक्ट्रॉनों की आबंधी युग्म तथा एकाकी युग्म से क्या समझते हैं? प्रत्येक को एक-एक उदाहरण द्वारा स्पष्ट कीजिए।
उत्तर:
इलेक्ट्रॉनों के वे युग्म आबन्धी युग्म कहलाते हैं जो दो परमाणुओं के मध्य साझा करके बन्ध बनाते हैं जबकि परमाणु पर उपस्थित वो इलेक्ट्रॉन युग्म जो बन्ध बनाने में भाग नहीं लेते हैं एकाकी इलेक्ट्रॉन युग्म कहलाते हैं।
उदाहरणार्थ:

प्रश्न 32.
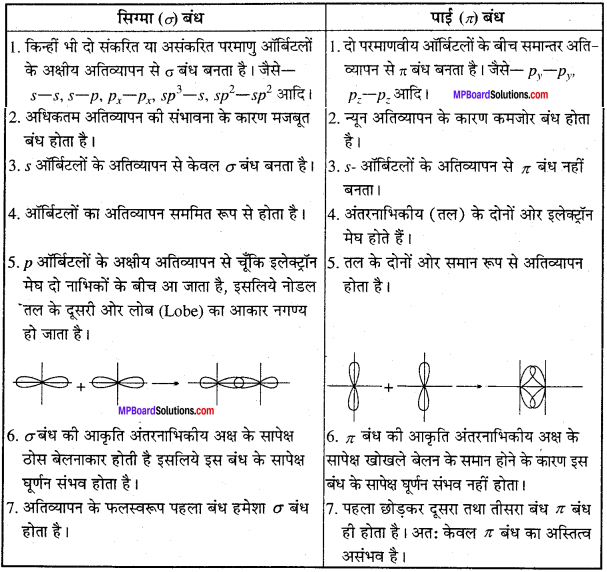
सिग्मा बंध तथा पाई आबंध में अंतर स्पष्ट कीजिए।
उत्तर:
>
प्रश्न 33.
संयोजकता आबंध सिद्धांत के आधार पर H2 अणु के विरचन की व्याख्या कीजिए।
उत्तर:
H2 अणु का बनना (s – s अतिव्यापन, σ बंध):
जब एक H – परमाणु का 1s ऑर्बिटल दूसरे H – परमाणु के 1s ऑर्बिटल, जिसके इलेक्ट्रॉन का चक्रण विपरीत हों, अतिव्यापन करते हैं तो अक्षीय अतिव्यापन होने के कारण मजबूत बंध (σ बंध) बनता है।
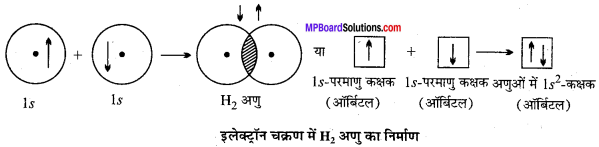
प्रश्न 34.
परमाणु कक्षकों के रैखिक संयोग से आण्विक कक्षक बनने के लिए आवश्यक शर्तों को लिखिए।
उत्तर:
परमाणु कक्षकों के रैखिक संयोग के लिए आवश्यक शर्ते निम्नानुसार हैं –
- संयोग करने वाले परमाणु कक्षकों की ऊर्जा लगभग समान होनी चाहिए।
- संयोग करने वाले परमाणु कक्षकों की आण्विक कक्ष के परितः समान सममिति होनी चाहिए।
- संयोग करने वाले परमाणु कक्षकों के मध्य अतिव्यापन पर्याप्त होना चाहिए।
प्रश्न 35.
आण्विक कक्षक सिद्धान्त के आधार पर समझाइए कि Be2 का अणु अस्तित्व क्यों नहीं होता?
उत्तर:
MOT के अनुसार Be2 अणु का अस्तित्व नहीं होता क्योंकि इस अणु के लिए बन्ध कोटि का मान शून्य प्राप्त होता है चूंकि Be का परमाणु क्रमांक 4 है अतः इसके अणु में 8 इलेक्ट्रॉन होंगे जिनका विन्यास अग्रानुसार होगा –
σls2, σ*1s2, σ2s2, σ*2s2
∴ बन्ध कोटि = \(\frac{1}{2}\) [Nb – Na] = \(\frac{1}{2}\) [4 – 4] = 0 बन्ध कोटि का मान शून्य है अत: Be2 अणु का अस्तित्व नहीं होगा।
प्रश्न 36.
निम्नलिखित स्पीशीज़ के आपेक्षिक स्थायित्व की तुलना कीजिए तथा उनके चुंबकीय गुण इंगित कीजिए –
O2, O2+, O2– (सुपर ऑक्साइड) तथा O (परऑक्साइड)।
उत्तर:
MOT के अनुसार O2 O2+, O2–, एवं O22- के बन्ध कोटि का मान क्रमश: 2, 2.5, 1.5 एवं 1 है। अत: इनके स्थायित्व का आपेक्षिक क्रम O2+ > O2 > O2– > O22- इनमें से O2, O22-; एवं O2–, अनुचुम्बकीय होंगे क्योंकि इनमें क्रमश: 2, 1, 1 अयुग्मित इलेक्ट्रॉन हैं। जबकि O, प्रतिचुम्बकीय होगा क्योंकि इसके सभी इलेक्ट्रॉन युग्मित हैं।
प्रश्न 37.
कक्षकों के निरूपण में प्रयुक्त धन (+) तथा ऋण (-) चिन्हों का क्या महत्व होता है?
उत्तर:
इलेक्ट्रॉन तरंग फलन में धन एवं ऋण चिन्ह, नाभिक से तरंग फलन की दिशा दर्शाते हैं। समान चिन्ह वाले तरंग फलनों के योग से आबंधी आण्विक कक्षक बनते हैं जबकि विपरीत चिन्ह वाले तरंग फलनों के योग से विपरीत बन्धी आण्विक कक्षक बनते हैं।
प्रश्न 38.
PCl5 अणु में संकरण का वर्णन कीजिए। इसमें अक्षीय आबंध विषुवतीय आबंधों की अपेक्षा अधिक लंबे क्यों होते हैं?
उत्तर:
sp3d संकरण – PCl5 का बनना:
PCl5 की आकृति त्रिकोणीय द्विपिरामिडीय है। स्पष्टतः इसमें एक,s, तीन p तथा एक d (यह dz2 होगा) संकरित होते हैं। पाँच नये spid संकरित ऑर्बिटलों में से तीन एक तल में 120° का कोण बनाते हुए तथा दो ऑर्बिटल, तल के ऊपर एवं नीचे 90° का कोण बनाते हुए रहेंगे।
फॉस्फोरस का इलेक्ट्रॉनिक विन्यास – (P का परमाणु क्रमांक 15 है तथा विन्यास 2, 8, 5 है)
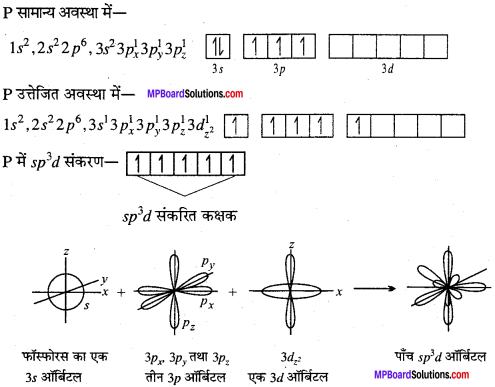
इस प्रकार से PCl5 में तीन P – Cl सिग्मा बंध एक तल में होते हैं, इन्हें निरक्षीय बंध तथा दो P – Cl बंध तल के लंबवत् ऊपर तथा नीचे होते हैं, इन्हें अक्षीय बंध कहते हैं।
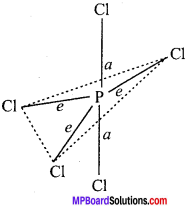
P – Cl विषुवतीय आबंध की लंबाई 2.04Å है जबकि P – Cl अक्षीय आबंध 2.19Å है। अक्षीय आबंध की लंबाई ज्यादा होने का कारण एकल-एकल इलेक्ट्रॉन युग्म में प्रतिकर्षण अधिक होता है। अतः प्रतिकर्षण के कारण अक्षीय आबंध की लंबाई अधिक है।
प्रश्न 39.
हाइड्रोजन आबंध की परिभाषा दीजिए। यह वाण्डर वाल्स बलों की अपेक्षा प्रबल होते हैं या दुर्बल?
उत्तर:
हाइड्रोजन बंध H – परमाणु व विद्युत्ऋणी परमाणु (N, O, F) के मध्य आकर्षण बल है। हाइड्रोजन बंध, वाण्डर वाल्स बलों की तुलना में प्रबल होता है क्योंकि हाइड्रोजन बंध में प्रबल द्विध्रुव-द्विध्रुव अन्योन्य क्रिया होती है जबकि वाण्डर वाल्स बल प्रकीर्णन का दुर्बल बल है।
प्रश्न 40.
‘आबंध कोटि’ से आप क्या समझते हैं? निम्नलिखित में आबंध-कोटि का परिकलन कीजिए –
N2, O2, O2+ तथा O2–.
उत्तर:
आबंध कोटि-अणु या आयन के दो परमाणुओं के बीच उपस्थित बंधों की संख्या आबंध कोटि (Bond order) कहलाती है।
![]()
उपर्युक्त सूत्र के आधार पर बंध कोटि के मान N2(3.0), O2(2.0), O2+(2.5) एवं O2– (1.5) होगा।
रासायनिक आबंधन तथा आण्विक संरचना अन्य महत्वपूर्ण प्रश्न
रासायनिक आबंधन तथा आण्विक संरचना वस्तुनिष्ठ प्रश्न
प्रश्न 1.
सही विकल्प चुनकर लिखिए –
प्रश्न 1.
समान परमाणुओं में सामान्यतः किस प्रकार का बन्ध बनता है
(a) आयनिक
(b) सहसंयोजक
(c) उप-सहसंयोजक
(d) धात्विक।
उत्तर:
(b) सहसंयोजक
प्रश्न 2.
अधिकतम द्विध्रुव आघूर्ण वाला अणु है –
(a) CH4
(b) CHCl3
(c) CHI3
(d) CCl4
उत्तर:
(b) CHCl3
प्रश्न 3.
अमोनिया में संकरण है –
(a) dsp2
(b) sp3
(c) sp2d
(d) d2sp.
उत्तर:
(b) sp3
प्रश्न 4.
जल का उच्च क्वथनांक निम्न कारण से होता है –
(a) जल के अणुओं का कम वियोजित होना
(b) जल के अणुओं के मध्य H-बंध होना
(c) जल की विशिष्ट ऊष्मा
(d) जल का उच्च डाइ-इलेक्ट्रिक स्थिरांक।
उत्तर:
(b) जल के अणुओं के मध्य H-बंध होना
प्रश्न 5.
किसका द्विध्रुव आघूर्ण शून्य है –
(a) H2O
(b) CO2
(c) SO2
(d) NO2
उत्तर:
(b) CO2
प्रश्न 6.
निम्न में से किस यौगिक में sp संकरित कक्षकों का उपयोग हुआ है –
(a) BCl3
(b) CH4
(c) NH3
(d) BeH2
उत्तर:
(a) BCl3
प्रश्न 7.
निम्न में से किसकी संरचना रैखिक है –
(a) CO2
(b) H2O
(c) SO2
(d) H2O2
उत्तर:
(a) CO2
प्रश्न 8.
PCI5 अणु निम्नलिखित संकरण का परिणाम है –
(a) sp2d2
(b) sp3d
(c) spd3
(d) sp2d3
उत्तर:
(b) sp3d
प्रश्न 9.
किस अणु में केन्द्रीय परमाणु के साथ बना बन्ध कोण अधिकतम होगा –
(a) NH3
(b) NH4
(c) PCl3
(d) SCl2
उत्तर:
(b) NH4
प्रश्न 10.
H-बंध उपस्थित है –
(a) CH4
(b) NaCl
(c) H2O
(d) CHCl3
उत्तर:
(c) H2O
प्रश्न 2.
रिक्त स्थानों की पूर्ति कीजिए –
- CH4 में ………….. संकरण पाया जाता है।
- LCAO का पूर्ण नाम है …………….।
- NH3 का क्वथनांक PH3 के क्वथनांक से …………. होता है।
- s – s अतिव्यापन से ……………….. बंध बनता है।
- जल के अणु में H – O – H बन्ध कोण …………….. होता है।
- p – p पाीय अतिव्यापन से …………….. बंध बनता है।
- रासायनिक बन्धों के निर्माण के साथ ऊर्जा में ……………. होती है।
- हीरा विद्युत् का ……………. है जबकि ग्रेफाइट ……………… है।
- ग्रेफाइट तथा हीरे में ……….. संकरण होता है।
- जल के अणु में …………….. संकरण होता है।
उत्तर:
- sp3
- लीनियर कॉम्बिनेशन ऑफ एटॉमिक ऑर्बिटल
- उच्च
- 6
- 104.5°
- 7
- कमी
- कुचालक, सुचालक
- sp2 व sp3
- sp3
प्रश्न 3.
उचित संबंध जोड़िए –

उत्तर:
- (c)
- (d)
- (e)
- (b)
- (a)
प्रश्न 4.
एक शब्द/वाक्य में उत्तर दीजिए –
- किस प्रकार के आबन्ध दिशात्मक होते हैं?
- सल्फर टेट्राफ्लोराइड की आकृति कैसी होती है?
- सोडियम क्लोराइड में किस प्रकार का रासायनिक बंध होता है?
- चीनी कार्बनिक यौगिक है फिर भी जल में विलेय है।
- जल के अणु का आबंध कोण है।
- BF अणु का द्विध्रुव आघूर्ण होता है।
उत्तर:
- सहसंयोजक बन्ध
- वर्ग पिरामीडीय
- विद्युत् संयोजी
- हाइड्रोजन बन्ध के कारण
- 104°5
- शून्य।
रासायनिक आबंधन तथा आण्विक संरचना अति लघु उत्तरीय प्रश्न
प्रश्न 1.
रासायनिक बंध किसे कहते हैं?
उत्तर:
सभी पदार्थों में परमाणु संयुक्त अवस्था में पाये जाते हैं तथा परमाणुओं के संयोग से विद्युत् आवेश रहित कण बनते हैं, वे अणु कहलाते हैं तथा किसी भी अणु में पाये जाने वाले परमाणुओं के मध्य पाये जाने वाला आकर्षण ही रासायनिक बंध कहलाता है।
प्रश्न 2.
संयोजकता का इलेक्ट्रॉनिक सिद्धांत क्या है? इसके मुख्य अभिगृहीत लिखिये।
उत्तर:
संयोजकता का इलेक्ट्रॉनिक सिद्धांत तथा इसके मुख्य अभिगृहीत निम्नलिखित हैं –
- किसी भी तत्व की संयोजकता उसके परमाणु के संयोजी कोश में उपस्थित इलेक्ट्रॉनों की संख्या पर निर्भर करती है।
- सभी तत्वों के परमाणुओं में अक्रिय गैस के समान स्थायी इलेक्ट्रॉनिक विन्यास प्राप्त करने की प्रवृत्ति होती है।
- किसी भी तत्व के संयोजी कोश में उपस्थित इलेक्ट्रॉन को संयोजी इलेक्ट्रॉन कहते हैं तथा जब इस संयोजी कोश से इलेक्ट्रॉन निकल जाते हैं तो बचा हुआ रिक्त कक्ष कर्नेल कहलाता है।
- यदि परमाणु अस्थायी हो तो वह स्थायित्व प्राप्त करने का प्रयास करता है।
इसके लिये वह इलेक्ट्रॉन का आदान-प्रदान या साझा करता है। इस आधार पर बंध तीन प्रकार के होते हैं –
- आयनिक बंध
- सहसंयोजी बंध
- उप-सहसंयोजी बंध।
प्रश्न 3.
आयनिक बंध बनाने के लिए अनुकूल कारकों को लिखिए।
उत्तर:
आयनिक आबंध बनाने के लिए अनुकूल कारक निम्न है –
- धनायन बनने वाले तत्व की आयनन एन्थैल्पी निम्न हो।
- ऋणायन बनने वाले तत्व की अधिक ऋणात्मक इलेक्ट्रॉन लब्धि एन्थैल्पी (इलेक्ट्रॉन बंधुता)।
- बनने वाले आयनिक यौगिक की उच्च जालक एन्थैल्पी।
प्रश्न 4.
निम्नलिखित अणुओं तथा आयनों की लुईस संरचनाएँ लिखिए –
H2S, SiCl4, BeF2, CO32-, HCOOH.
उत्तर:
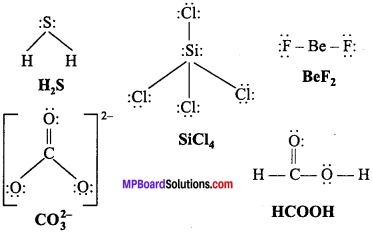
प्रश्न 5.
निम्नलिखित तत्वों के परमाणुओं के लुईस बिंदु प्रतीक लिखिए –
Mg, Br, Na, O.
उत्तर:

प्रश्न 6.
निम्नलिखित परमाणुओं से इलेक्ट्रॉन स्थानांतरण द्वारा धनायनों और ऋणायनों में विरचन को लुईस बिन्दु प्रतीकों की सहायता में दर्शाइए –
(a) K तथा S
(b) Ca तथा O
(c) AI तथा N.
उत्तर:

प्रश्न 7.
लुईस प्रतीक क्या है? निम्नलिखित में से प्रत्येक तत्व का लुईस प्रतीक लिखिए –
Na, Ca, B, Br, Xe, C, A, O.
उत्तर:
गिलबर्ट न्यूटन लुईस ने परमाणु में उपस्थित संयोजकता इलेक्ट्रॉन को दर्शाने के लिये लुईस प्रतीक का उपयोग किया। इस विधि में किसी परमाणु के संयोजी कोश में उपस्थित इलेक्ट्रॉन को दर्शाने के लिये उस तत्व के प्रतीक के चारों ओर उतने ही बिन्दु दर्शाते हैं, जितने इलेक्ट्रॉन उसके बाह्य संयोजी कोश में उपस्थित रहते हैं।

प्रश्न 8.
एकाकी इलेक्ट्रॉन युग्म से क्या समझते हैं?
उत्तर:
किसी परमाणु के संयोजी कोश में उपस्थित इलेक्ट्रॉन युग्म जो बंध निर्माण में भाग नहीं लेता है। अर्थात् बंध निर्माण के पश्चात् संयोजी कोश में उपस्थित इलेक्ट्रॉन युग्म जो परमाणु में शेष रहता है, एकाकी इलेक्ट्रॉन युग्म कहलाता है। जैसे – H2O अणु में केन्द्रीय परमाणु ऑक्सीजन के पास दो एकाकी इलेक्ट्रॉन युग्म होते हैं।
![]()
बंध युग्म = 2, एकाकी इलेक्ट्रॉन युग्म = 2
प्रश्न 9.
द्विध्रुव आघूर्ण से क्या समझते हैं?
उत्तर:
किसी बंध का द्विध्रुव आघूर्ण परमाणुओं पर उपस्थित आवेश की मात्रा तथा उनके बीच की दूरी के गुणनफल के बराबर होता है। यह एक सदिश राशि है तथा इसकी सहायता से किसी बंध की आयनिक प्रतिशतता की गणना की जा सकती है। इसे µ से दर्शाते हैं।
µ = e x d
जहाँ µ = द्विध्रुव आघूर्ण
e = आवेश की मात्रा
d = परमाणुओं के बीच की दूरी।
इसकी इकाई डिबाई होती है, इसे D से दर्शाते हैं।
ID = 10-18 cm-e.s.u.
प्रश्न 10.
आबंध ऊर्जा या बंध ऊर्जा किसे कहते हैं?
उत्तर:
किसी द्विपरमाणुक अणु की बंधन ऊर्जा वह ऊर्जा है जो दो उदासीन परमाणुओं के बंधित होकर उसके एक ग्राम अणु को गैसीय अवस्था में आने पर मुक्त होता है।
A + B → A – B + ऊर्जा
दूसरे शब्दों में, एक ग्राम अणु पदार्थ की गैसीय अवस्था में दो परमाणुओं के बीच बने सहसंयोजक बंध को तोड़ने के लिये जितनी ऊर्जा की आवश्यकता होती है, उसे बंधन ऊर्जा कहते हैं। आबन्ध ऊर्जा का मात्रक किलो कैलोरी प्रति जूल या किलो जूल प्रति मोल है।
प्रश्न 11.
BrF5– की आकृति की व्याख्या कीजिए।
उत्तर:
BrF5– में केन्द्रीय परमाणु Br (35Br = 2, 8, 18, 7) के संयोजी कोश में सात इलेक्ट्रॉन उपस्थित होते हैं, जिनमें से पाँच इलेक्ट्रॉन, पाँच फ्लुओरीन (F) परमाणुओं के साथ आबंध बनाते हैं तथा शेष दो इलेक्ट्रॉन एकाकी युग्म के रूप में रहते हैं। अतः कुल छः युग्म (पाँच आबंधी युग्म तथा एक एकाकी युग्म) उपस्थित होते हैं। एकाकी युग्म और आबंधी युग्म के मध्य प्रतिकर्षण को न्यूनतम करने के लिए, इसकी आकृति वर्ग-पिरामिडीय हो जाती है।
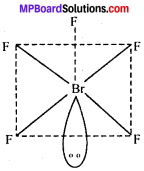
प्रश्न 12.
कक्षकों के निरूपण में उपयुक्त धन (+) तथा ऋण (-) चिह्नों का क्या महत्व होता है?
उत्तर:
परमाणु कक्षक तरंग फलन के रूप में दर्शाये जाते हैं। कक्षक में धन (+) चिह्न, धन तरंग फलन को तथा ऋण चिह्न (-), ऋण तरंग फलन को प्रदर्शित करता है। समान चिह्न वाले दो तरंग फलनों के संयोग से आबंध आण्विक बंध बनते हैं। जबकि विपरीत चिह्न वाले दो तरंग फलनों के संयोग से प्रति आबंध आण्विक कक्षक बनते हैं।
प्रश्न 13.
निम्नलिखित अणुओं में सिग्मा (σ) तथा पाई (π) आबंधों की कुल संख्या कितनी है –
(a) C2H2
(b) C2H4
उत्तर:

प्रश्न 14.
हाइड्रोजन बंध से क्या समझते हैं?
उत्तर:
किसी अणु में उपस्थित सहसंयोजी बंध द्वारा जुड़े हाइड्रोजन परमाणु और उसी यौगिक के अन्य अणु के प्रबल ऋण विद्युती तत्व के बीच कार्य कर रहे स्थिर वैद्युत आकर्षण बल को हाइड्रोजन बंध कहते हैं, इसे बिन्दुकित रेखा द्वारा दर्शाते हैं। हाइड्रोजन बंध दो प्रकार के होते हैं –
- अन्तर अणुक हाइड्रोजन बंध,
- अन्तःअणुक हाइड्रोजन बंध।
प्रश्न 15.
सामान्य ताप पर जल द्रव होता है, जबकि हाइड्रोजन सल्फाइड गैस है, क्यों?
उत्तर:
H2O तथा H2S, ऑक्सीजन तथा सल्फर के हाइड्रोजन के साथ बने यौगिक हैं। जल में उपस्थित ऑक्सीजन प्रबल ऋणविद्युती तत्व है। इसलिये साधारण ताप पर जल के अणुओं के मध्य अन्तर अणुक हाइड्रोजन बंध का बनना संभव है। इस अंतर अणुक हाइड्रोजन बंध के कारण जल के अणु संगुणित होते हैं जिसके कारण साधारण ताप पर जल द्रव है तथा इसके क्वथनांक उच्च होते हैं।
H2S में उपस्थित (S) के बड़े आकार के कारण ऋणविद्युतता कम होती है इसलिये H2S अणु के मध्य हाइड्रोजन बंध का बनना संभव नहीं है इसलिये इनके अणुओं के मध्य केवल दुर्बल वाण्डर वाल्स आकर्षण बल होता है अत: H2S साधारण ताप पर गैस है।
प्रश्न 16.
ग्लिसरॉल की श्यानता एथेनॉल से अधिक है, क्यों?
उत्तर:
एथेनॉल अणु में एक हाइड्रॉक्सिल समूह होता है जबकि प्रत्येक ग्लिसरॉल में तीन OH समूह होते हैं जो तीन हाइड्रोजन बंध बनाते हैं अर्थात् ग्लिसरॉल में हाइड्रोजन बंध बनाने की प्रवृत्ति एथेनॉल से अधिक है। इसलिये ग्लिसरॉल की श्यानता एथेनॉल से अधिक है।
प्रश्न 17.
सल्फ्यूरिक अम्ल के उच्च क्वथनांक तथा उच्च श्यानता का कारण स्पष्ट कीजिए।
उत्तर:
H2SO4 अणु में उच्च ऋणविद्युतता होने के कारण हाइड्रोजन बंध बनाने की प्रवृत्ति होती है। H-बंध के कारण H2SO4 के अणु संगुणित अवस्था में होते हैं। इस अंतर अणुक हाइड्रोजन बंध के कारण ये सरलता से वाष्पित नहीं होते हैं इसलिये इनके क्वथनांक तथा श्यानता उच्च होती है।
प्रश्न 18.
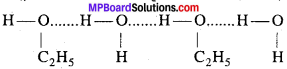
एथिल एल्कोहॉल की जल में विलेयता का क्या कारण है?
उत्तर:
एथिल एल्कोहॉल जल के अणुओं के साथ सरलता से अंतर अणुक हाइड्रोजन बंध का निर्माण कर सकते हैं इस हाइड्रोजन बंध बनाने की प्रवृत्ति के कारण एथिल एल्कोहॉल जल में सरलता से विलेय है।
प्रश्न 19.
किसी अणु द्वारा हाइड्रोजन बंध निर्माण के लिये प्रमुख शर्ते क्या हैं?
उत्तर:
किसी अणु द्वारा हाइड्रोजन बंध बनने की शर्ते निम्नलिखित हैं –
- किसी अणु में हाइड्रोजन से जुड़े सहसंयोजी बंध द्वारा जुड़े परमाणु की ऋणविद्युतता अत्यधिक उच्च होनी चाहिए।
- हाइड्रोजन से सहसंयोजी बंध द्वारा जुड़े परमाणु की परमाणु त्रिज्या कम होनी चाहिये।
प्रश्न 20.
जालक ऊर्जा और जलयोजन ऊर्जा से क्या समझते हैं?
उत्तर:
1. जालक ऊर्जा:
किसी आयनिक ठोस की जालक ऊर्जा, वह ऊर्जा है जो एक-दूसरे से अनन्त दूरी पर स्थित अवयवी गैसीय आयनों से एक मोल ठोस क्रिस्टल बनने से उत्सर्जित होती है। दूसरे शब्दों में, किसी भी क्रिस्टल के निर्माण में निकलने वाली ऊर्जा को जालक ऊर्जा कहते हैं।
2. जलयोजन ऊर्जा:
किसी आयन को जल में विलेय करने पर या आयन के साथ जल के संयुक्त होने पर निकलने वाली ऊर्जा जलयोजन ऊर्जा कहलाती है।
प्रश्न 21.
परमाण्वीय कक्षकों के अतिव्यापन के लिये किन परिस्थितियों का होना आवश्यक है?
उत्तर:
परमाण्वीय कक्षकों के अतिव्यापन के लिये निम्नलिखित परिस्थितियों का होना आवश्यक है –
- दोनों परमाण्वीय कक्षकों की ऊर्जा लगभग समान होनी चाहिए।
- दोनों परमाणुओं के नाभिकों की अक्ष पर एक-सी सममिति होनी चाहिये।
- किसी भी संयोग के लिये अतिव्यापन की एक निश्चित सीमा आवश्यक है अर्थात् अतिव्यापन की सीमा अधिकतम होनी चाहिये।
प्रश्न 22.
(सिग्मा) σ बंध किसे कहते हैं?
उत्तर:
जब अर्धपूर्ण कक्षक एक-दूसरे के साथ सम्मुख अतिव्यापन करते हैं तो बंध बनता है। इस प्रकार का बंध s – s, S – p तथा p – p कक्षकों के सम्मुख अतिव्यापन के फलस्वरूप बनते हैं। यह प्रबलतम बंध है तथा इलेक्ट्रॉनों का घनत्व अंतः नाभिकीय अक्ष पर अधिकतम होता है।
प्रश्न 23.
σ – बंध, π – बंध की तुलना में प्रबल होता है, क्यों?
उत्तर:
किसी भी बंध की प्रबलता अतिव्यापन की सीमा पर निर्भर करती है। σ बंध सम्मुख अतिव्यापन के फलस्वरूप बनते हैं जबकि π बंध पार्श्व अतिव्यापन के फलस्वरूप बनते हैं। इसलिये बंध में अतिव्यापन की सीमा बंध से अधिक होती है क्योंकि अणु में उपस्थित बंध की उपस्थिति के कारण दोनों परमाणुओं के मध्य एक न्यूनतम दूरी निर्धारित होती है। जिसके कारण ग बंध निर्माण के दौरान कक्षक अधिकतम अतिव्यापन नहीं कर सकते हैं। इसलिये π बंध, σ बंध की तुलना में दुर्बल हैं।

प्रश्न 24.
HCl एक सहसंयोजी यौगिक है, फिर भी इसका जलीय विलयन आयनित क्यों हो जाता है?
उत्तर:
HCl सहसंयोजी यौगिक है लेकिन HCl में क्लोरीन की ऋणविद्युतता H से अधिक है जिसके कारण साझे का इलेक्ट्रॉन युग्म क्लोरीन की ओर विस्थापित हो जाता है, जिसके फलस्वरूप H पर आंशिक धन आवेश तथा Cl पर आंशिक ऋण आवेश उत्पन्न हो जाता है। अर्थात् HCl अणु में ध्रुवता उत्पन्न हो जाती है एवं बंध दुर्बल हो जाते हैं। HCl को जल में घोलने पर जल के अणु H+ और Cl– के बीच आकर्षण बल को कम कर देते हैं और HCl सरलता से आयनित हो जाता है।
प्रश्न 25.
विद्युत् संयोजी तथा सहसंयोजी यौगिकों में से किनके क्वथनांक उच्च होते हैं, और क्यों?
उत्तर:
विद्युत् संयोजी यौगिकों के क्रिस्टल आयनों से मिलकर बने होते हैं तथा इन आयनों के बीच प्रबल स्थिर वैद्युत आकर्षण बल होता है, जिसके कारण ये दृढ़ता से बँधे रहते हैं तथा इनको पृथक् करने के लिये तथा वाष्पित करने के लिये अधिक ऊर्जा की आवश्यकता होती है। इसलिये वैद्युत संयोजी यौगिकों के क्वथनांक सहसंयोजी यौगिक से उच्च होते हैं क्योंकि सहसंयोजी यौगिक परमाणु के संयोजन से बनते हैं तथा इनके मध्य केवल दुर्बल वाण्डर वाल्स आकर्षण बल होता है।
प्रश्न 26.
BaSO4, जल में अविलेय है, क्यों?
उत्तर:
किसी आयनिक यौगिक की जल में विलेयता जालक ऊर्जा तथा जलयोजन ऊर्जा पर निर्भर करती है। यदि किसी यौगिक की जालक ऊर्जा जलयोजन ऊर्जा से अधिक हो, तो वह आयनिक यौगिक जल में अविलेय होता है। BaSO4, की जालक ऊर्जा का मान जलयोजन ऊर्जा के मान से अधिक है, इसलिये BaSO4 जल में अविलेय है।
प्रश्न 27.
SO3, NO2, तथा NO3– की अनुनाद संरचनाएँ लिखिए।
उत्तर:
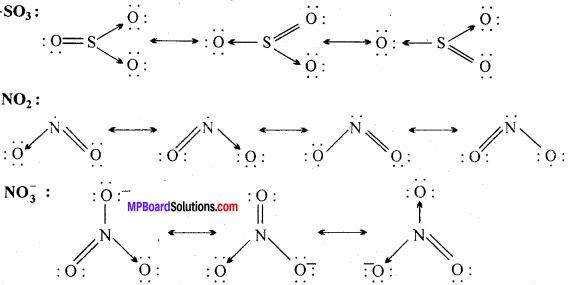
प्रश्न 28.
सोडियम एक प्रबल विद्युत् धनात्मक तत्व है, क्यों?
उत्तर:
सोडियम का परमाणु क्रमांक 11 है तथा इनका इलेक्ट्रॉनिक विन्यास 2, 8, 1 है। इसके बड़े आकार के कारण इनकी आयनन ऊर्जा का मान अत्यन्त कम होता है, जिसके फलस्वरूप ये सरलता से इलेक्ट्रॉन का त्याग कर धनायन बनाते हैं। इसलिये ये प्रबल धनविद्युती तत्व हैं।
प्रश्न 29.
विद्युत् संयोजक बंध किस प्रकार के यौगिकों के मध्य बनता है?
उत्तर:
प्रबल धन विद्युतीय तत्व तथा प्रबल ऋणविद्युती तत्वों के मध्य आयनिक बंध बनता है क्योंकि प्रबल धन विद्युती तत्व सरलता से इलेक्ट्रॉन त्याग कर धनायन बनाते हैं जबकि प्रबल ऋणविद्युती तत्व सरलता से इलेक्ट्रॉन ग्रहण कर ऋणायन बनाते हैं। ये धन आयन तथा ऋण आयनों के मध्य प्रबल स्थिर वैद्युत आकर्षण बल होता है। इस प्रबल स्थिर वैद्युत आकर्षण बल को ही वैद्युत संयोजी या आयनिक बंध कहते हैं।
उदाहरण – Na2,8,1 + Cl2,8,7 → Na2,8+ Cl2,8,8–
प्रश्न 30.
HF अणु HI अणु से अधिक ध्रुवीय है, क्यों?
उत्तर:
फ्लुओरीन की ऋणविद्युतता आयोडीन से अधिक होती है, इसलिये साझे के इलेक्ट्रॉनों का विस्थापन-HF में HI की तुलना में अधिक होता है, जिसके फलस्वरूप HF में आवेश का विभाजन HI से अधिक है, इसलिये HF अणु HI से अधिक ध्रुवीय है।
प्रश्न 31.
C – CI बंध ध्रुवीय होता है, किन्तु CCl4 अध्रुवीय होता है। कारण स्पष्ट कीजिए।
उत्तर:
C – CI बंध में क्लोरीन की ऋणविद्युतता C की तुलना में उच्च है, जिसके कारण साझे के इलेक्ट्रॉन क्लोरीन की ओर विस्थापित हो जाते हैं जिससे C पर आंशिक धन आवेश तथा CI पर आंशिक ऋण आवेश आ जाता है और यह बंध ध्रुवीय प्रकृति दर्शाता है।
जबकि CCl4 अणु की संरचना सममित होती है, जिसके कारण C – Cl बंधों के द्विध्रुव आघूर्ण एकदूसरे को निरस्त कर देते हैं, इसलिये CCl4 का अणु अध्रुवीय होता है।
प्रश्न 32.
अनुनाद से क्या समझते हैं?
उत्तर:
जब किसी अणु को एक निश्चित संरचना सूत्र द्वारा व्यक्त नहीं किया जा सकता अर्थात् उस संरचना सूत्र के द्वारा उसके समस्त गुणों का स्पष्टीकरण नहीं किया जा सकता बल्कि अणु के अभिलाक्षणिक गुणों की व्याख्या दो या दो से अधिक विभिन्न संरचना सूत्रों द्वारा की जाये तो इस घटना को अनुनाद कहते हैं तथा ये सभी संरचना सूत्र अनुनाद संरचना सूत्र या कैलॉनिकल रूप कहलाते हैं।
प्रश्न 33.
अनुनाद की प्रमुख शर्ते क्या हैं?
उत्तर:
अनुनाद के लिये आवश्यक शर्ते निम्नलिखित हैं –
- सभी अनुनादी रूपों की संभवन ऊष्माएँ लगभग बराबर होती हैं।
- प्रत्येक सूत्र में परमाणुओं की व्यवस्था समान होनी चाहिये।
- सभी अनुनादी रूपों में अयुग्मित इलेक्ट्रॉनों की संख्या बराबर होनी चाहिये।
प्रश्न 34.
अनुनाद ऊर्जा से क्या समझते हैं?
उत्तर:
अणु की वास्तविक ऊर्जा और सूत्र द्वारा गणना की गयी ऊर्जाओं में अंतर होता है। इन दोनों ऊर्जाओं के अंतर को अनुनादी ऊर्जा कहते हैं। दूसरे शब्दों में, अनुनाद संकर और सर्वाधिक स्थायी अनुनाद संरचना की ऊर्जा का अंतर, अनुनाद ऊर्जा कहलाता है। अनुनाद ऊर्जा का मान जितना अधिक होता है, अणु उतना ही अधिक स्थायी होता है।
प्रश्न 35.
N2 के बंध कोटि की गणना कीजिए।
उत्तर:
N2 (14 इलेक्ट्रॉन) का इलेक्ट्रॉनिक विन्यास –
σ1s, σ*1s2, σ2s2, σ*2s2, (π2px2 = π2py2), σ2pz2
आबंध कोटि = =(Nb – Na) = x (10 – 4) = 3
प्रश्न 36.
संकरण की परिभाषा लिखिये।
उत्तर:
परमाणु के संयोजी कोश में उपस्थित लगभग समान ऊर्जा वाले कक्षक आपस में ऊर्जा का पुनर्विन्यास कर समान ऊर्जा तथा समान आकार वाले उतनी ही संख्या में नये कक्षकों का निर्माण करते हैं, यह प्रक्रिया संकरण कहलाती है।
प्रश्न 37.
s तथा p कक्षक में अंतर लिखिये।
उत्तर:
s तथा p कक्षक में अंतर:
s – कक्षक:
- ये कक्षक गोलतः सममित होते हैं।
- ये अदिशात्मक होते हैं।
- इनके लिये l = 0 तथा m = 0 होता है।
p – कक्षक:
- ये कक्षक डम्बल के आकार के होते हैं तथा अपने अक्ष पर सममित होते हैं।
- ये दिशात्मक होते हैं।
- इनके लिये l = 1 तथा m = -1, 0, +1 होता है।
प्रश्न 38.
जल का क्वथनांक HF से उच्च होता है जबकि फ्लुओरीन की ऋणविद्युतता ऑक्सीजन से अधिक है। कारण स्पष्ट कीजिए।
उत्तर:
HF के एक अणु में एक फ्लुओरीन के साथ एक H जुड़ा है जिसके कारण प्रत्येक HF अणु दो हाइड्रोजन बंध बना सकता है जबकि HO के अणु में ऑक्सीजन परमाणु दो हाइड्रोजन के साथ जुड़ा है जिसके कारण प्रत्येक जल का अणु चार हाइड्रोजन बंध बना सकता है। इस प्रकार जल में H बंध बनाने की प्रवृत्ति HF से अधिक है। इसलिये जल का क्वथनांक HF से अधिक है।
प्रश्न 39.
उपसहसंयोजी यौगिकों के गुण लिखिए।
उत्तर:
उपसहसंयोजी यौगिकों के गुण निम्नलिखित हैं –
- यह प्रायः जल में अविलेय होते हैं किन्तु कार्बनिक विलायकों में विलेय होते हैं।
- उपसहसंयोजक बंध दृढ़ और दिशात्मक होते हैं।
- इनके क्वथनांक एवं गलनांक वैद्युत संयोजी यौगिक से कम लेकिन सहसंयोजी यौगिकों से अधिक होते हैं।
प्रश्न 40.
निम्नांकित अणुओं की ज्यामितीय आकृति का प्रकार तथा बन्ध कोण का मान लिखिए –
1. C2H2,
2. BCl3
3. NH3
4. PCl5
उत्तर:
ज्यामितीय आकृति का प्रकार तथा बन्ध कोण का मान –
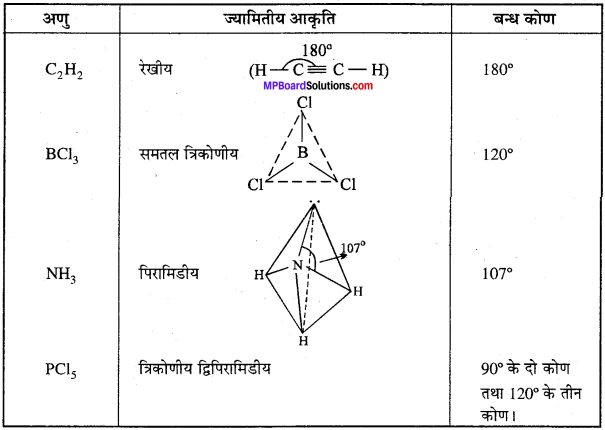
प्रश्न 41.
निम्नांकित की अनुनादी संरचनाएँ बनाइये –
1. NO3⊖
2. CO2
उत्तर:
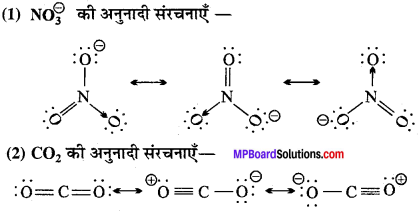
रासायनिक आबंधन तथा आण्विक संरचना लघु उत्तरीय प्रश्न
प्रश्न 1.
आयनिक बंध का बनना किन कारकों पर निर्भर करता है?
उत्तर:
आयनिक बंध का बनना निम्नलिखित कारकों पर निर्भर करता है –
- ऋणविद्युतता – संयोग करने वाले दोनों परमाणुओं की ऋणविद्युतता में अत्यधिक अंतर होना चाहिये। इस अंतर का मान जितना अधिक होगा, बंध का आयनिक गुण उतना ही अधिक होगा।
- आयनन ऊर्जा – इलेक्ट्रॉन दान करने वाले परमाणु अर्थात् धातु की आयनन ऊर्जा का मान अत्यन्त कम होना चाहिये, जिससे धातु सरलता से इलेक्ट्रॉन दान कर धनायन बनायेगा।
- इलेक्ट्रॉन बंधुता – इलेक्ट्रॉन ग्रहण करने वाले परमाणु की इलेक्ट्रॉन बंधुता उच्च होनी चाहिये, जिससे परमाणु सरलता से इलेक्ट्रॉन ग्रहण कर ऋणायन बनायेगा।
- जालक ऊर्जा – यौगिक की जालक ऊर्जा का मान जितना अधिक होगा यौगिक की आयनिक प्रवृत्ति उतनी ही अधिक होगी।
प्रश्न 2.
संकरण के नियम लिखिए।
उत्तर:
संकरण के नियम –
- संकरण में भाग लेने वाले कक्षकों की ऊर्जा लगभग समान होनी चाहिए।
- संकरण के पश्चात् प्राप्त होने वाले संकरित कक्षकों की संख्या संकरण में भाग लेने वाले कक्षकों की संख्या के बराबर होती है।
- संकरण में केवल कक्षक भाग लेते हैं इलेक्ट्रॉन नहीं।
- अर्धपूर्ण, पूर्ण तथा अपूर्ण कक्षक संकरण में भाग लेते हैं।
- किसी भी अणु की ज्यामिति, बंध कोण संकरण पर निर्भर करता है।
- संकरण एक परिकल्पना है, जिसका उपयोग प्रायोगिक तथ्यों के स्पष्टीकरण के लिये किया जाता है।
प्रश्न 3.
सहसंयोजी बंध को उदाहरण सहित समझाइये।
उत्तर:
दो या दो से अधिक परमाणुओं के मध्य इलेक्ट्रॉनों की साझेदारी से जो बंध बनते हैं, सहसंयोजी बंध कहलाते हैं। साझे के इलेक्ट्रॉन दोनों परमाणुओं के केन्द्र में रहते हैं तथा इन पर दोनों परमाणुओं का समान अधिकार रहता है। एक-एक, दो-दो या तीन-तीन इलेक्ट्रॉनों के साझे से क्रमशः एकल बंध, द्विबंध तथा त्रिबंध बनता है।
उदाहरण – Cl2 अणु का बनना –
क्लोरीन का इलेक्ट्रॉनिक विन्यास 2, 8, 7 है। इसके संयोजी कोश में 7 इलेक्ट्रॉन हैं, इसे अपना अष्टक पूर्ण करने के लिये एक अतिरिक्त इलेक्ट्रॉन की आवश्यकता है। यह क्लोरीन दूसरे क्लोरीन परमाणु के साथ एक इलेक्ट्रॉन का साझा करके अपना अष्टक पूर्ण करता है । इस प्रकार क्लोरीन अणु (Cl,) में दो क्लोरीन परमाणु के मध्य एकल बंध होता है।
![]()
प्रश्न 4.
अध्रुवीय और ध्रुवीय सहसंयोजी बंध में क्या अंतर है?
उत्तर:
अध्रुवीय सहसंयोजी बंध:
जब सहसंयोजी बंध दो ऐसे परमाणुओं के मध्य बनता है, जिनकी ऋणविद्युतता बराबर है तो साझे के इलेक्ट्रॉन युग्म दोनों परमाणुओं के केन्द्र में रहते हैं, इस प्रकार बने बंध को अध्रुवीय सहसंयोजी बंध कहते हैं।
उदाहरण –

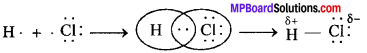
ध्रुवीय सहसंयोजी बंध:
जब सहसंयोजी बंध दो ऐसे परमाणुओं के मध्य बनता है, जिनकी ऋणविद्युतता में अंतर है तो साझे के इलेक्ट्रॉन अधिक ऋणविद्युती तत्व की ओर विस्थापित होता है, जिसके फलस्वरूप अधिक ऋणविद्युती तत्व पर आंशिक ऋण आवेश तथा कम ऋणविद्युती तत्व पर आंशिक धन आवेश आ जाता है। इस प्रकार के सहसंयोजी बंध को अध्रुवीय सहसंयोजी बंध कहते हैं।
प्रश्न 5.
सहसंयोजी यौगिक के विशिष्ट गुण बताइये।
उत्तर:
सहसंयोजी यौगिक के गुण निम्नलिखित हैं –
- सहसंयोजी यौगिक सामान्यतः गैस या द्रव अवस्था में होते हैं लेकिन उच्च अणुभार वाले यौगिक ठोस होते हैं।
- इनके गलनांक एवं क्वथनांक निम्न होते हैं।
- ये अध्रुवीय विलायकों में विलेय होते हैं।
- ये विद्युत् के कुचालक होते हैं।
- ये बंध दृढ़ एवं दिशात्मक होते हैं।
- इनके अणुओं के मध्य रासायनिक अभिक्रिया मंद होती है क्योंकि बंधों के टूटने में तथा नये बंधों के बनने में समय लगता है।
प्रश्न 6.
विद्युत् संयोजी (आयनिक) यौगिक एवं सहसंयोजी यौगिक में अंतर लिखिये।
उत्तर:
विद्युत् संयोजी (आयनिक) यौगिक एवं सहसंयोजी यौगिक में अंतर –
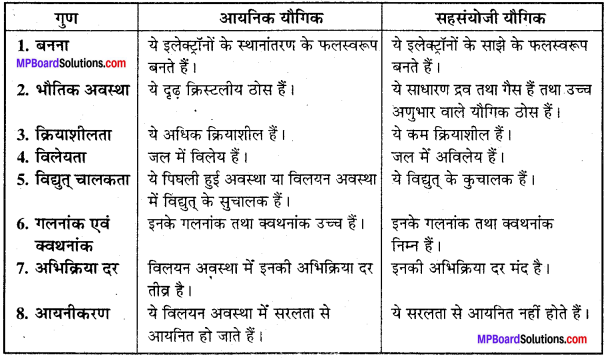
प्रश्न 7.
बर्फ जल से हल्की होती है, क्यों? समझाइये।
अथवा,
बर्फ का घनत्व जल से कम है, क्यों?
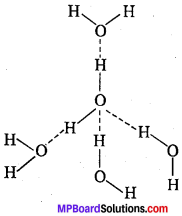
उत्तर:
बर्फ के क्रिस्टल बनते समय अणुओं में परस्पर हाइड्रोजन बंध इस प्रकार व्यवस्थित होते हैं कि जल का एक अणु चार अणुओं के साथ चतुष्फलकीय रूप से घिरा रहता है जिसमें दो H सहसंयोजी बंध द्वारा तथा अन्य दो H, हाइड्रोजन बंध द्वारा जुड़े रहते हैं, जिसके फलस्वरूप खुले पिंजरे जैसी संरचना बनती हैं और जालक के मध्य खाली स्थान रहता है, ho इसलिये बर्फ का घनत्व जल से कम होता है, जिसके कारण बर्फ जल से H हल्की होती है।
प्रश्न 8.
उपसहसंयोजी बंध को उदाहरण सहित समझाइये।
उत्तर:
उपसहसंयोजी बंध एक विशिष्ट प्रकार का सहसंयोजी बंध है जिसमें साझे का इलेक्ट्रॉन जोड़ा एक परमाणु या अणु का होता है जिसका अष्टक पूर्ण होता है तथा दूसरा परमाणु या अणु जिसका अष्टक अपूर्ण होता है वह बिना साझे में योगदान के इस इलेक्ट्रॉन युग्म को ग्रहण करता है। इस जोड़े पर दोनों परमाणु का समान अधिकार होता है। इलेक्ट्रॉन जोड़ा दान देने वाले परमाणु या अणु को दाता कहते हैं और ग्रहण करने वाले परमाणु को ग्राही कहते हैं। इस प्रकार बने बंध को उपसहसंयोजी बंध या दाता-ग्राही बंध कहते हैं तथा तीर (-) चिन्ह द्वारा दर्शाते हैं।
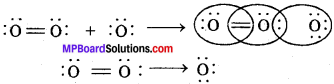
उदाहरण – O3 का बनना:
O2, अणु में दोनों ऑक्सीजन अणुओं का अष्टक पूर्ण रहता है तथा दोनों ऑक्सीजन के पास दो इलेक्ट्रॉन युग्म हैं जबकि तीसरे ऑक्सीजन परमाणु के संयोजी कोश में 6 इलेक्ट्रॉन हैं तथा इसे अष्टक पूर्ण करने के लिये 2 इलेक्ट्रॉन की आवश्यकता होती है। इसलिये O2 अणु अपना एक एकाकी इलेक्ट्रॉन इस ऑक्सीजन परमाणु को दान कर उपसहसंयोजी बंध बनाता है।
प्रश्न 9.
क्या निम्नलिखित अभिक्रिया के फलस्वरूप B तथा N परमाणुओं की संकरण-अवस्था में परिवर्तन होता है?
BF3 + NH3 + F3B.NH3
उत्तर:
BF3 में 3 आबंध युग्म तथा O एकाकी युग्म होते हैं। जिनके कारण बोरॉन sp2 संकरित होती है तथा NH3 में 3 आबंध युग्म तथा 1 एकाकी युग्म की उपस्थिति के कारण, नाइट्रोजन sp3 संकरित होता है। अभिक्रिया के पश्चात् बोरॉन का संकरण sp3 में परिवर्तित हो जाता है परन्तु नाइट्रोजन का संकरण समान ही रहता है क्योंकि N अपने एकाकी युग्म को इलेक्ट्रॉनों की कमी वाले B के साथ साझेदारी करता है।
प्रश्न 10.
निम्नलिखित अभिक्रिया में Al परमाणु की संकरण अवस्था में परिवर्तन ( यदि होता है, तो) को समझाइए।
AlCl3 + Cl– → AlCl4–
उत्तर:
Al का इलेक्ट्रॉनिक विन्यास निम्नलिखित है –
आद्य (सामान्य) अवस्था में 13A1 = 1s2, 2s2 2p6, 3s23px1
उत्तेजित अवस्था में = 1s2, 2s22p6, 3s2, 3px1,3py1
AlCl3 के निर्माण में Al sp2 संकरित होता है तथा इसकी ज्यामितीय त्रिकोणीय समतलीय होती है। दूसरी ओर AlCl4– के निर्माण में रिक्त 3pz कक्षक सम्मिलित होने के कारण, Al sp3 संकरित होता है तथा इसकी ज्यामितीय चतुष्फलकीय होती है।
प्रश्न 11.
धात्विक बंध क्या है? उदाहरण देकर स्पष्ट कीजिए।
उत्तर:
धात्विक बंध की व्याख्या करने के लिये धातुओं में उपस्थित बंध के दो सिद्धांत हैं –
1. स्वतंत्र इलेक्ट्रॉन सिद्धांत:
यह सिद्धांत सन् 1900 में ड्रड द्वारा दिया गया था तथा सन् 1916 में लारेन्ज द्वारा विकसित किया गया। इस सिद्धांत के अनुसार, “धात्विक ठोस धनायनों का वह समूह है जो गतिशील इलेक्ट्रॉनों के द्रव अथवा समुद्र में व्यवस्थित ढंग से डूबा हुआ है तथा वह बल जो इन धनायनों को इलेक्ट्रॉन समुद्र में बाँधे रखता है, धात्विक बंध कहलाता है।”
उदाहरण – Mg धातु का प्रत्येक परमाणु 2 इलेक्ट्रॉन दान करके Mg+2 आयनों का जालक बनाता है तथा इसके संयोजी इलेक्ट्रॉनों से इलेक्ट्रॉन समुद्र बनता है।
2. संयोजकता बंध सिद्धांत:
इस सिद्धांत के अनुसार, “ धातुओं में बंध सहसंयोजी प्रकृति का होता है तथा उनमें अनुनाद पाया जाता है।”
उदाहरण:
प्रत्येक Li परमाणु आठ अन्य Li परमाणु द्वारा घिरा रहता है तथा यह बारी-बारी से प्रत्येक Li के साथ सहसंयोजी बंध बनाता है, इस प्रकार कई अनुनादी संरचनाएँ प्राप्त होती हैं ।

प्रश्न 12.
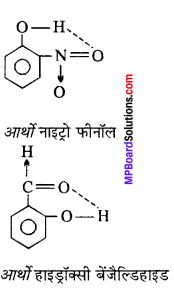
अन्तराअणुक तथा अन्तःअणुक हाइड्रोजन बंध को उदाहरण सहित समझाइये।
उत्तर:
अंतराअणुक हाइड्रोजन बंध:
जब दो या अधिक समान अथवा भिन्न अणुओं के मध्य हाइड्रोजन बंध बनता है तो इसे अन्तराअणुक हाइड्रोजन बंध कहते हैं। इसमें एक अणु का हाइड्रोजन दूसरे अणु के प्रबल ऋण विद्युती परमाणु के साथ हाइड्रोजन बंध बनाता है।
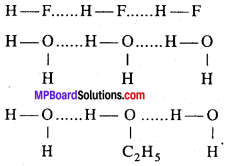
अन्तःअणुक हाइड्रोजन बंध:
जब एक ही यौगिक के एक ही अणु के भिन्न-भिन्न स्थिति पर भिन्नभिन्न बंधों से जुड़े परमाणुओं के मध्य H बंध बनता है, तो उसे अन्तःअणुक हाइड्रोजन बंध कहते हैं।
प्रश्न 13.
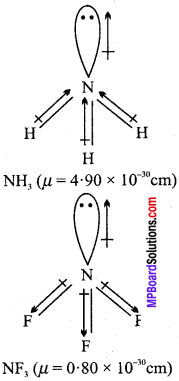
NH3 तथा NF3 में किस अणु का द्विध्रुव-आघूर्ण अधिक है और क्यों?
उत्तर:
NH3 तथा NF3 दोनों अणुओं का आकार पिरामिडीय होता है, परन्तु NH3 का द्विध्रुव आघूर्ण NF3 की अपेक्षा अधिक होता है। NH3 में एकाकी युग्म इलेक्ट्रॉन युग्म का द्विध्रुव, तीन N – H बन्धों की दिशा में ही होता है, जबकि NF, में एकाकी युग्म का द्विध्रुव, तीन N – F बन्धों की विपरीत दिशा में होता है जिसके कारण NF3 का द्विध्रुव आघूर्ण का मान घट जाता है।
प्रश्न 14.
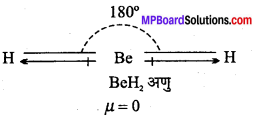
यद्यपि Be-H आबंध ध्रुवीय है, तथापि BeH2 अणु का द्विध्रुव आघूर्ण शून्य है। स्पष्ट कीजिए।
उत्तर:
BeH2 अणु रेखीय होता है। विपरीत दिशाओं में स्थित दो समान आबंध द्विध्रुव, एक दूसरे के प्रभाव को समाप्त कर देते हैं। यही कारण है कि BeH, अणु का द्विध्रुव आघूर्ण शून्य होता है।
प्रश्न 15.
सहसंयोजी बंध के परमाणु कक्षक अतिव्यापन सिद्धांत की प्रमुख अभिधारणाएँ कौनकौन सी हैं?
उत्तर:
इस सिद्धांत के अनुसार:
- जब एक परमाणु का कक्षक दूसरे परमाणु के कक्षक से अतिव्यापन करता है तो सहसंयोजी बंध बनते हैं।
- बंध बनने पर बंधी इलेक्ट्रॉन दोनों परमाणुओं के नाभिक से सम्बन्धित होता है।
- आबंधी इलेक्ट्रॉनों का चक्रण विपरीत दिशा में होना चाहिये।
- बंध का सामर्थ्य अतिव्यापन की मात्रा पर निर्भर करता है।
- अतिव्यापन के आधार पर बंध दो प्रकार के होते हैं- बंध तथा 7 बंध।
- किसी भी तत्व की संयोजकता उसके संयोजी कोश में उपस्थित अयुग्मित इलेक्ट्रॉनों की संख्या पर निर्भर करती है।
- अतिव्यापन उन्हीं कक्षकों में होता है जो बंध निर्माण में भाग लेते हैं।
- एक से अधिक अयुग्मित इलेक्ट्रॉनों वाले कक्षकों के अतिव्यापन से बहु आबन्ध बनते हैं।
प्रश्न 16.
कारण स्पष्ट करते हुए निम्न यौगिकों को उनके बढ़ते हुए आयनिक व्यवहार के क्रम में व्यवस्थित कीजिए –
N – H, F – H, C – H तथा O – H
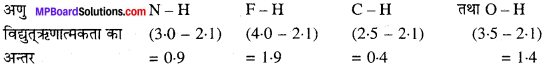
अत: आयनिक व्यवहार का सही क्रम निम्न होगा
C – H < N – H < O – H < F – H
प्रश्न 17.
स्पष्ट कीजिए कि PCl5 त्रिकोणीय द्विपिरामिडीय तथा IF, वर्ग पिरामिडीय क्यों है?
उत्तर:
PCl5 – इसमें फॉस्फोरस (Z = 15) केन्द्रीय परमाणु है जिसके आद्य अवस्था तथा उत्तेजित अवस्था में इलेक्ट्रॉनिक विन्यास निम्नवत हैं।
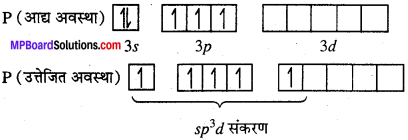
PCl5 में, फॉस्फोरस spid संकरित है अतः इसकी ज्यामितीय त्रिकोणीय द्विपिरामिडीय होगी।
IF5 – इसमें केन्द्रीय परमाणु आयोडीन (z = 53) है जिसके आद्य (Ground) अवस्था तथा उत्तेजित अवस्था में इलेक्ट्रॉनिक विन्यास अग्रवत है –
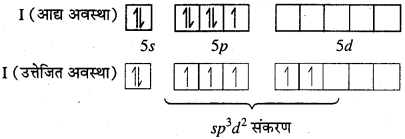
IF5 में, आयोडीन spid संकरित है अतः इसकी ज्यामितीय वर्ग पिरामिडीय होगी। विकृति एकाकी इलेक्ट्रॉन के कारण होती है।
प्रश्न 18.
σ बंध और n बंध किसे कहते हैं? उदाहरण देकर समझाइये।
उत्तर:
σ बंध:
जब दो अर्धपूर्ण कक्षक एक ही अक्ष पर कक्षकों के सम्मुख अतिव्यापन करते हैं तो बनने वाले बंध को बंध कहते हैं। σ बंध में इलेक्ट्रॉन घनत्व अंतर नाभिकीय अक्ष पर अधिकतम होता है, यह प्रबलतम बंध है। σ – बंध s – s अतिव्यापन, s – p अतिव्यापन तथा p – p कक्षकों के सम्मुख अतिव्यापन के फलस्वरूप बनता है।
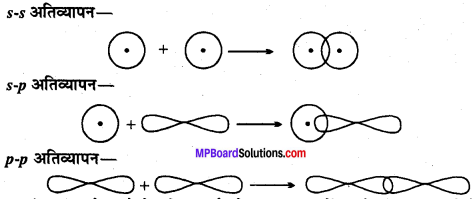
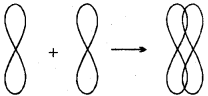
π बंध:
जब दो या दो से अधिक अर्धपूर्ण कक्षक आपस में पार्श्व अतिव्यापन करते हैं तो सबंध बनता है। यह बंध दुर्बल बंध है। 1 बंध का बनना तभी संभव है जब अणु में पहले से बंध उपस्थित होता है।
प्रश्न 19.
VSEPR सिद्धांत के आधार पर निम्नलिखित यौगिकों के संकरण एवं आकृतियाँ बताइये –
SnCl2, SiCl4, SF4, H2S, HF, NCl3, PCI5, XeF2, NH3, H2O.
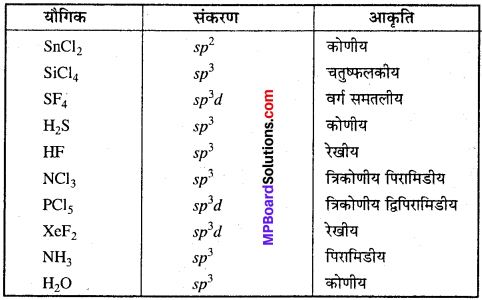
प्रश्न 20.
निम्नलिखित अणुओं में कार्बन परमाणु कौन-से संकर कक्षक प्रयुक्त करते हैं –
(a) CH3 – CH3
(b) CH3CH = CH2
(c) CH3CH2OH
(d) CH3CHO
(e) CH2COOH.
उत्तर:
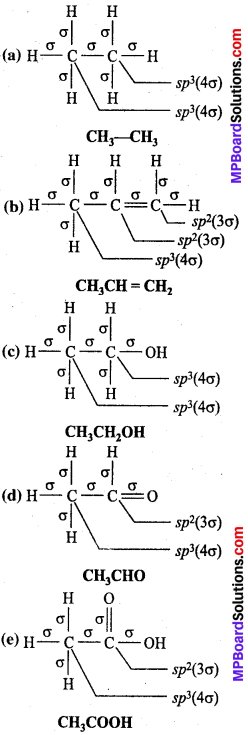
प्रश्न 21.
इलेक्ट्रॉनों के आबंधी युग्म तथा एकाकी युग्म से आप क्या समझते हो? प्रत्येक को एक उदाहरण द्वारा स्पष्ट कीजिए।
उत्तर:
सहसंयोजी आबंध इलेक्ट्रॉनों की आपसी साझेदारी द्वारा बनता है। आबंधित परमाणुओं के मध्य साझे का इलेक्ट्रॉन युग्म, आबंधी युग्म कहलाता है। वे इलेक्ट्रॉन जो आबंध निर्माण में भाग नहीं लेते हैं, एकाकी युग्म कहलाते हैं।
उदाहरण – अमोनिया (NH3) में 3 आबंध युग्म तथा 1 एकाकी इलेक्ट्रॉन युग्म उपस्थित होते हैं। जल (H2O) में 2 आबंध युग्म तथा 2 एकाकी इलेक्ट्रॉन युग्म उपस्थित होते हैं। मेथेन (CH4) में केवल 4 आबंध युग्म इलेक्ट्रॉन उपस्थित होते हैं।
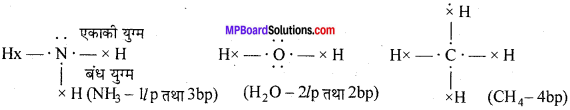
प्रश्न 22.
S – s अतिव्यापन क्या है? उदाहरण सहित समझाइये।
उत्तर:
जब एक परमाणु का अर्धपूर्ण s – कक्षक दूसरे परमाणु के अर्धपूर्ण s-कक्षक के साथ सम्मुख अतिव्यापन कर σ बंध बनाता है तो इसे S – S अतिव्यापन कहते हैं। यह बंध नाभिकीय अक्ष के चारों ओर सममित होता है।
उदाहरण – H2 अणु का बनना – H परमाणु का परमाणु क्रमांक 1 है। इसका सामान्य इलेक्ट्रॉनिक विन्यास 1s1 है। H2 अणु निर्माण के दौरान H परमाणु का अर्धपूर्ण s – कक्षक, दूसरे H परमाणु के अर्धपूर्ण sकक्षक के साथ सम्मुख अतिव्यापन कर σ बंध बनाता है।
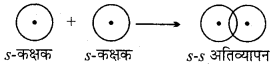
प्रश्न 23.
s – p अतिव्यापन क्या है? उदाहरण सहित समझाइये।
उत्तर:
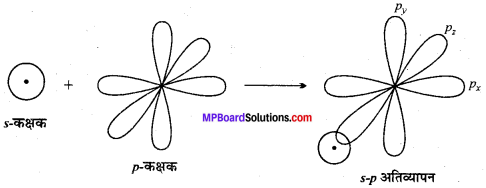
जब किसी एक परमाणु का अर्धपूर्ण s – कक्षक किसी दूसरे परमाणु के अर्धपूर्ण p कक्षक के साथ सम्मुख अतिव्यापन कर – बंध बनाता है तो इसे s – p अतिव्यापन कहते हैं।
उदाहरण – HCl अणु का बनना – Cl का इलेक्ट्रॉनिक विन्यास 1s22s22p63s23p5 है। HCl अणु के निर्माण के दौरान Cl परमाणु का अर्धपूर्ण pz कक्षक H के अर्धपूर्ण s-कक्षक के साथ सम्मुख अतिव्यापन कर σ बंध बनाता है।
प्रश्न 24.
कार्बन के दो अपरूप हीरा और ग्रेफाइट के गुणों में अंतर का कारण स्पष्ट कीजिए।
उत्तर:
हीरा तथा ग्रेफाइट दोनों कार्बन के अपरूप हैं लेकिन C की व्यवस्था में भिन्नता के कारण इनके गुणों में अंतर होता है। हीरा में C परमाणु sp2 संकरित अवस्था में है तथा प्रत्येक C अन्य चार कार्बन परमाणुओं के साथ जुड़कर चतुष्फलकीय संरचना बनाता है। इस प्रकार यह एक त्रिविमीय संरचना बनाता है इसलिये हीरा कठोर है तथा इसका गलनांक उच्च है।
ग्रेफाइट में प्रत्येक C, sp2 संकरित अवस्था में है अर्थात् प्रत्येक अन्य तीन C परमाणु द्वारा घिरा रहता है तथा प्रत्येक C की चौथी संयोजकता असंतृप्त रहती है। ग्रेफाइट में विभिन्न परतें होती हैं जो आपस में दुर्बल वाण्डर वाल्स आकर्षण बल द्वारा जुड़ी रहती हैं इसलिये ग्रेफाइट कोमल है तथा मुक्त इलेक्ट्रॉन की उपस्थिति के कारण यह विद्युत् का सुचालक है।
प्रश्न 25.
x – अक्ष को अंतर्नाभिकीय अक्ष मानते हुए बताइए कि निम्नलिखित में कौन-से कक्षक सिग्मा (σ) आबंध नहीं बनाएँगे और क्यों?
(a) 1s तथा 1s
(b) 1s तथा 2p
(c) 2py तथा 2pz
(d) 1s तथा 25
उत्तर:
केवल (c), σ आबंध नहीं बनाएँगे क्योंकि X – अक्ष को अंतर्नाभिकीय अक्ष लेने पर 2p, तथा 2p, अक्षों के मध्य पार्श्व अतिव्यापन होता है जिसके फलस्वरूप T- आबंध बनता है।
प्रश्न 26.
चतुष्फलकीय ज्यामिति के अलावा CH4 अणु की एक और संभव ज्यामिति वर्गसमतलीय है, जिसमें हाइड्रोजन के चार परमाणु एक वर्ग के चार कोनों पर होते हैं। व्याख्या कीजिए कि CH4 का अणु वर्ग-समतलीय नहीं होता है।
उत्तर:
कार्बन का इलेक्ट्रॉनिक विन्यास निम्नलिखित है –

CH4 अणु में, कार्बन sp3 संकरित होता है जिसके कारण इसकी ज्यामिति चतुष्फलकीय होती है। वर्गसमतलीय ज्यामिति के लिए dsp2 संकरण आवश्यक होता है। परन्तु कार्बन में d – कक्षकों की अनुपस्थिति के कारण यह संभव नहीं है। साथ ही, VSEPR सिद्धान्त के अनुसार, कार्बन परमाणु के परितः चार आबन्ध इलेक्ट्रॉन चतुष्फलकीय ज्यामिति में स्थित होते हैं। चतुष्फलकीय संरचना में, आबंध कोण 109° 28′ तथा वर्गसमतलीय ज्यामिति में 90° का होता है। अतः चतुष्फलकीय ज्यामिति में आबंध इलेक्ट्रॉनों का प्रतिकर्षण वर्गसमतलीय ज्यामिति की तुलना में कम होता है।
प्रश्न 27.
संकरण के आधार पर स्पष्ट कीजिये कि BeCl2 अणु की संरचना रेखीय होती है।
उत्तर:
BeCl2 में Be, sp संकरित अवस्था में है।
sp संकरण:
जब s का एक कक्षक तथा p उपकोश का 1 कक्षक आपस में ऊर्जा के पुनर्विन्यास द्वारा दो संकरित कक्षकों का निर्माण करते हैं तो इसे sp संकरण कहते हैं।
BeCl2 अणु की आकृति:
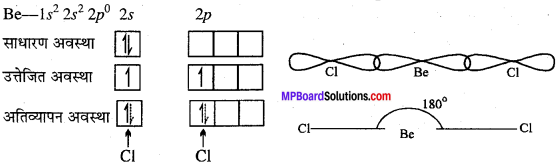
BeCl2 में Be केन्द्रीय परमाणु है, इसका सामान्य इलेक्ट्रॉनिक विन्यास 1s22s22p0 है। उत्तेजित अवस्था में 25 कक्षक का एक इलेक्ट्रॉन उत्तेजित होकर रिक्त 2p उपकोश में चला जाता है। 2s का 1 कक्षक तथा 2p का 1 कक्षक आपस में ऊर्जा के पुनर्विन्यास द्वारा दो संकरित कक्षकों का निर्माण करते हैं जो एक-दूसरे से 180° का कोण बनाते हुये व्यवस्थित रहते हैं। ये दोनों संकरित कक्षक दो क्लोरीन परमाणु के साथ सम्मुख अतिव्यापन कर दो बंध बनाते हैं इसलिये BeCl2 की संरचना रेखीय होती है।
प्रश्न 28.
sp3 संकरण क्या है? उदाहरण देकर स्पष्ट कीजिये।
उत्तर:
sp3 संकरण:
जब 5 उपकोश का कक्षक तथा p उपकोश के तीन कक्षक आपस में ऊर्जा के पुनर्विन्यास द्वारा चार संकरित कक्षकों का निर्माण करते हैं तो इसे sp3 संकरण कहते हैं। प्रतिकर्षण के कारण ये चारों त्रिविम में एक-दूसरे के साथ 109°28′ का कोण बनाते हैं अर्थात् ये चारों कक्षक समचतुष्फलक के चारों कोनों की ओर निर्देशित रहते हैं।
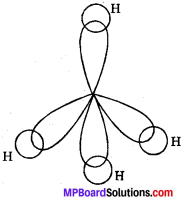
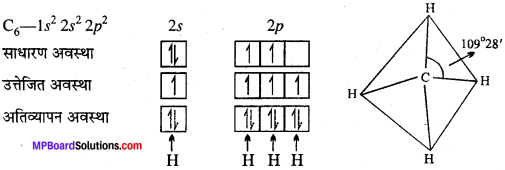
उदाहरण – CH4 – कार्बन का परमाणु क्रमांक 6 है तथा इसका सामान्य इलेक्ट्रॉनिक विन्यास 1s22s42p2 है। उत्तेजित अवस्था में 2s का एक इलेक्ट्रॉन उत्तेजित होकर रिक्त 2pz कक्षक में चला जाता है। इस प्रकार उत्तेजित अवस्था में C के पास चार अयुग्मित इलेक्ट्रॉन होते हैं। कार्बन का 2s कक्षक तथा 2p उपकोश के तीनों कक्षक आपस में ऊर्जा के पुनर्विन्यास द्वारा चार संकरित कक्षकों का निर्माण करते हैं, जो चार हाइड्रोजन परमाणुओं के H साथ सम्मुख अतिव्यापन कर चार बंध बनाते हैं। sp3 संकरण के कारण मेथेन अणु की संरचना समचतुष्फलकीय होती है तथा बंध कोण का मान 109°28′ होता है।
प्रश्न 29.
उपसहसंयोजी बंध के आधार पर HNO3 तथा H2SO4 की संरचना समझाइये।
उत्तर:
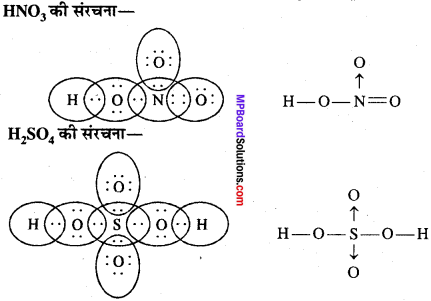
प्रश्न 30.
परमाणु कक्षकों के रैखिक संयोग से आण्विक कक्षक बनने के लिए आवश्यक शर्तों को लिखें।
उत्तर:
परमाणु कक्षकों के रैखिक संयोग से आण्विक कक्षकों के निर्माण के लिए निम्नलिखित शर्ते आवश्यक है –
1. संयोग करने वाले परमाणु कक्षकों की ऊर्जा समान या लगभग समान होनी चाहिए। उदाहरण के लिए 1s – कक्षक केवल 1s – कक्षक में संयोग करेगा, 25 कक्षक से नहीं क्योंकि 2s – कक्षक की ऊर्जा, 1s – कक्षक की अपेक्षा अधिक होती है। इस प्रकार का संयोग तभी संभव है जबकि संयोग करने वाले परमाणु भिन्न हो (अंतर्नाभिकीय द्विपरमाणुक अणु)
2. संयोग करने वाले परमाणु कक्षकों की आण्विक कक्ष के परितः समान सममिति होनी चाहिए। उदाहरण के लिए, किसी परमाणु का 2pz कक्षक दूसरे परमाणु के 2px कक्षक से ही संयोग करेगा, परन्तु यह 2py तथा 2pz से ही नहीं कर सकता है क्योंकि उनकी सममितियाँ समान नहीं है।
3. संयोग करने वाले परमाणु कक्षकों को अधिकतम अतिव्यापन करना चाहिए। कक्षकों के मध्य जितना अधिक अतिव्यापन होगा, उनके नाभिकों के बीच इलेक्ट्रॉन घनत्व उतना ही अधिक होगा।

प्रश्न 31.
कक्षक सिद्धांत या अतिव्यापन के आधार पर N2 अणु का बनना समझाइये।
उत्तर:
N परमाणु का परमाणु क्रमांक 7 है, इसका सामान्य इलेक्ट्रॉनिक विन्यास 1s22s22p3 है। इसके संयोजी कोश के p उपकोश में तीन अयुग्मित इलेक्ट्रॉन हैं तथा इसे अपना अष्टक पूर्ण करने के लिये तीन अतिरिक्त इलेक्ट्रॉन की आवश्यकता है। N परमाणु का px कक्षक, दूसरे N परमाणु के py कक्षक के साथ सम्मुख अतिव्यापन कर σ बंध बनाता है तथा दोनों नाइट्रोजन के px तथा py कक्षक आपस में पार्श्व अतिव्यापन कर दो π बंध बनाते हैं, इस प्रकार N अणु में दोनों N परमाणु के मध्य त्रिक बंध बनता है।

प्रश्न 32.
अणु कक्षक सिद्धांत के मुख्य बिन्दुओं को स्पष्ट कीजिए।
उत्तर:
अणु कक्षक सिद्धांत के मुख्य बिन्दु:
- परमाणुओं के परमाणु कक्षक संयोग करके अणु कक्षक बनाते हैं।
- परमाणु कक्षकों के रेखीय संयोग से आण्विक कक्षक का बनना माना जाता है।
- आण्विक कक्षक दो प्रकार के होते हैं –
- बंधी आण्विक कक्षक (Bonding molecular orbital) यह तरंग फलनों के योग से बनते हैं।
- विपरीत बंधी आण्विक कक्षक (Anti-bonding molecular orbital) ये तरंग फलनों के अन्तर से बनते हैं।
- आण्विक कक्षक बहुकेन्द्रीय (Polycentric) होते हैं अत: इलेक्ट्रॉन दो या दो से अधिक नाभिकों के द्वारा प्रभावित होते हैं।
- अन्दर की कक्षाओं के परमाणु कक्षक (संयोजी कक्षक के अतिरिक्त) भी संयोग करके आण्विक कक्षक बनाते हैं।
इन्हें सामान्यतया अनाबंधी (Non-bonding) आण्विक कक्षक कहते हैं। आण्विक कक्षक का बनना अतिव्यापन के द्वारा होता है। इलेक्ट्रॉनों के भरने में ऑफबाऊ सिद्धांत, हुण्ड के नियम एवं अन्य नियमों का पालन होता है।
प्रश्न 33.
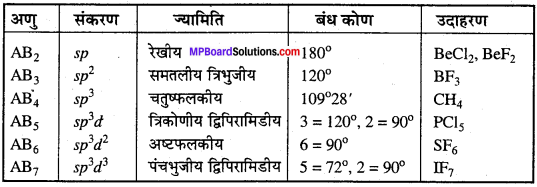
निम्नलिखित यौगिकों में उपस्थित संकरण, ज्यामिति तथा बंध कोण लिखिये।
उत्तर:
यौगिकों में संकरण,ज्यामिति तथा बंध कोण –
रासायनिक आबंधन तथा आण्विक संरचना दीर्घ उत्तरीय प्रश्न
प्रश्न 1.
द्विध्रुव आघूर्ण के महत्वपूर्ण अनुप्रयोग बताइए।
उत्तर:
द्विध्रुव आघूर्ण के महत्वपूर्ण अनुप्रयोग निम्न हैं –
1. द्विध्रुव आघूर्ण की सहायता से ज्ञात होता है कि दिया गया अणु ध्रुवीय है अथवा अध्रुवीय। द्विध्रुव आघूर्ण का मान (µ = e x d) जितना अधिक होता है, अणु उतना ही अधिक ध्रुवीय होता है। अध्रुवीय अणुओं के लिए, द्विध्रुव आघूर्ण का मान शून्य होता है।
उदाहरण – CO2
2. इसकी सहायता से आयनिक व्यवहार का प्रतिशत निम्न प्रकार से ज्ञात कर सकते हैं –

3. सममित अणुओं का द्विध्रुव आघूर्ण शून्य होता है। यद्यपि उनमें दो या अधिक ध्रुवीय बंध होते हैं। अतः अणु के सममितता के मापन में प्रयोग होता है।
4. इसकी सहायता से समपक्ष (Cis) तथा विपक्ष (Trans) समावयवियों में विभेद किया जा सकता है। सामान्यतः विपक्ष समावयवी की तुलना में समपक्ष समावयवी का द्विध्रुव आघूर्ण अधिक होता है।
5. ऑर्थो (Ortho), मेटा (Meta), तथा पैरा (Para) समावयवियों में विभेद करने में भी इसका प्रयोग होता है। पैरा समावयवी का द्विध्रुव आघूर्ण शून्य होता है। ऑर्थो समावयवी का द्विध्रुव आघूर्ण, मेटा समावयवी की अपेक्षा अधिक होता है।
6. अणुओं के आकार के बारे में जानकारी प्राप्त होती है।
प्रश्न 2.
संयोजकता कोश इलेक्ट्रॉन युग्म प्रतिकर्षण सिद्धांत क्या है? इसकी सीमायें बताइये। अथवा, संयोजकता कोश इलेक्ट्रॉन युग्म प्रतिकर्षण सिद्धांत को उदाहरण सहित समझाइये।
उत्तर:
सहसंयोजी अणुओं की ज्यामिति VSEPR सिद्धांत के आधार पर स्पष्ट की जा सकती है। इस सिद्धांत के अनुसार –
1. किसी अणु की ज्यामिति केन्द्रीय परमाणु के संयोजी कोश में उपस्थित बंधी तथा एकाकी इलेक्ट्रॉन युग्म या अनआबन्धी इलेक्ट्रॉन युग्म की संख्या पर निर्भर करती है।
2. अणु के केन्द्रीय परमाणु के संयोजी कोश में केवल बन्धित इलेक्ट्रॉन युग्म होने पर अणु की ज्यामितीय सममित होती है तथा अणु की ज्यामिति संकरण के प्रकार पर निर्भर करती है। यदि संयोजकता कोश में क्रमशः 2, 3, 4, 5, 6 तथा 7 बंधी इलेक्ट्रॉन युग्म हैं तो अणु की ज्यामिति क्रमशः रेखीय, समतलीय त्रिभुजीय, समचतुष्फलकीय, त्रिभुजीय द्विपिरामिडीय, अष्टफलकीय तथा पंचभुजीय द्विपिरामिडीय होती है।
3. यदि अणु के केन्द्रीय परमाणु के संयोजी कोश में बंधी तथा एकाकी इलेक्ट्रॉन युग्म उपस्थित हो तो अणु की ज्यामितीय सममित नहीं रहती है क्योंकि इलेक्ट्रॉन युग्म की उपस्थिति के कारण बंधी तथा एकाकी इलेक्ट्रॉन युग्म में अधिक प्रतिकर्षण होता है, जिसके कारण अणु की ज्यामिति नष्ट हो जाता है, विभिन्न इलेक्ट्रॉन युग्मों में प्रतिकर्षण का क्रम निम्नलिखित होता है,
Lone pair – Lone pair > Lone pair – Bond pair > Bond pair – Bond pair.
4. केन्द्रीय परमाणु पर एकाकी इलेक्ट्रॉन युग्मों की संख्या में वृद्धि करने पर बंधी इलेक्ट्रॉन युग्मों के मध्य बंध कोण का मान कम हो जाता है।
5. केन्द्रीय परमाणु के संयोजकता कोश में यदि इलेक्ट्रॉन पूर्ण भरा है तो उसके बन्धित इलेक्ट्रॉन युग्मों में प्रतिकर्षण अपूर्ण संयोजकता कोश के बन्धित इलेक्ट्रॉन युग्मों के प्रतिकर्षण से अधिक होता है।
सीमायें:
- इस सिद्धांत के आधार पर संक्रमण धातुओं के जटिल लवणों के आकृतियों की घोषणा नहीं की जा सकती है।
- इस सिद्धांत की सहायता से ऐसे अणुओं की आकृतियों को नहीं समझाया जा सकता जिसमें बहुत अधिक सीमा में विस्थानीकृत π इलेक्ट्रॉन है। अत्यधिक ध्रुवीय यौगिक जैसे, Li2o की आकृति की व्याख्या नहीं की जा सकती है।
उदाहरण:
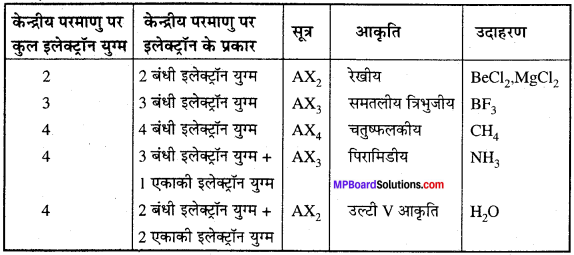
प्रश्न 3.
निम्नलिखित स्पीशीज के आपेक्षिक स्थायित्व की तुलना कीजिए तथा उनके चुंबकीय गुण इंगित कीजिए –
O2, O2+, O2– (सुपर ऑक्साइड) तथा O22- (पर ऑक्साइड)
उत्तर:
स्पीशीज के इलेक्ट्रॉनिक विन्यास निम्न है –
(a) O2(16 e–) →
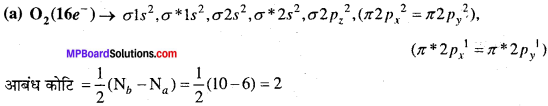
O2+ में दो अयुग्मित इलेक्ट्रॉन होने के कारण यह अनुचुम्बकीय है।
(b) O2+ आयन O2 अणु में से 1 इलेक्ट्रॉन निकलने के कारण बनता है।
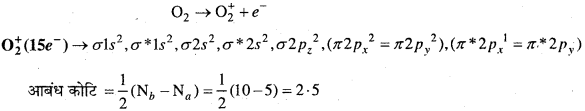
O2+ में एक इलेक्ट्रॉन अयुग्मित है अत: अनुचुम्बकीय होगा।
(c) O2– (सुपर ऑक्साइड) आयन – O2, अणु में 1 इलेक्ट्रॉन के योग से बनता है।
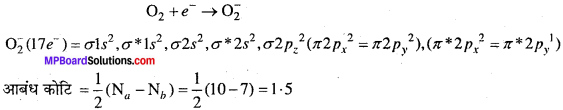
O2– आयन में 1 अयुग्मित इलेक्ट्रॉन उपस्थित होने के कारण अनुचुम्बकीय होता है।
(d) O2-2 (परऑक्साइड) आयन O2 अणु में 2 इलेक्ट्रॉन के योग से बनता है।
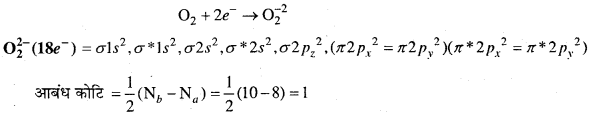
O2 में सभी इलेक्ट्रॉन युग्मित होने के कारण यह प्रतिचुम्बकीय है।
स्थायित्व का घटता क्रम – हम जानते हैं कि आबंध कोटि स्थायित्व
अतः स्थायित्व का घटता हुआ क्रम निम्न है – O2+ > O2 > O2– > O2-2
प्रश्न 4.
हाइड्रोजन आबन्धन किसे कहते हैं ? यह यौगिकों के गुणों को किस प्रकार प्रभावित करता है?
उत्तर:
किसी अणु के हाइड्रोजन परमाणु तथा किसी समान अथवा विभिन्न प्रकार के दूसरे अणु के प्रबल विद्युत् ऋणात्मक परमाणु जैसे – O, F तथा N के बीच आकर्षण बल को हाइड्रोजन बंध कहते हैं। दूसरे शब्दों. में, वह स्थिर वैद्युत आकर्षण बल जो किसी यौगिक के अणु में उपस्थित सहसंयोजी बंध द्वारा जुड़े हाइड्रोजन परमाणु और उसी यौगिक के अन्य अणु के प्रेबल विद्युत् ऋणात्मक परमाणु के बीच बनता है। इसे बिन्दुकित रेखा द्वारा दर्शाते हैं, यह बंध सहसंयोजक बंध की तुलना में दुर्बल है।
हाइड्रोजन बंध का प्रभाव:
हाइड्रोजन बंध यौगिकों के भौतिक एवं रासायनिक गुणों जैसे-क्वथनांक, विलेयता इत्यादि को प्रभावित करता है। अंतराअणुक हाइड्रोजन बंध के कारण अणु संगुणित होते हैं इसलिये इनके गलनांक तथा क्वथनांक उच्च होते हैं। जबकि अन्तः अणुक हाइड्रोजन बंध के कारण यौगिकों के गलनांक, क्वथनांक, विलेयता इत्यादि कम हो जाते हैं।
उदाहरण:
भौतिक अवस्था:
1. H2O में हाइड्रोजन बंध के कारण जल के अणु संगुणित अवस्था में होते हैं इसलिये साधारण ताप पर H2O द्रव है जबकि H2S में के कम ऋणविद्युती होने के कारण हाइड्रोजन बंध का बनना संभव नहीं है। इनके अणुओं के मध्य दुर्बल वाण्डर वाल्स आकर्षण बल होता है इसलिये साधारण ताप पर H2S गैस है।
2. विलेयता:
एल्कोहॉल तथा कार्बोक्सिलिक अम्ल सरलता से जल के साथ अंतरा अणुक हाइड्रोजन बंध बना लेते हैं इसलिये ये जल में विलेय हैं।
प्रश्न 5.
सहसंयोजी बंध के बनने को स्थिर वैद्युत आकर्षण तथा प्रतिकर्षण बल के आधार पर समझाइये।
अथवा
हाइड्रोजन अणु के लिये सहसंयोजी क्वाण्टम सिद्धांत क्या है? समझाइये।
उत्तर:
सहसंयोजी बंध निर्माण के दौरान जब दो परमाणु एक-दूसरे के निकट आते हैं तो उनके मध्य दो प्रकार के बल कार्य करते हैं।
- दोनों परमाणुओं के नाभिकों के द्वारा एक-दूसरे के इलेक्ट्रॉन अणु के प्रति आकर्षण।
- दोनों परमाणुओं के नाभिकों के मध्य तथा दोनों परमाणुओं के इलेक्ट्रॉनों के मध्य प्रतिकर्षण बल।
जब कार्यशील आकर्षण बल एवं प्रतिकर्षण बल का परिणामी बल आकर्षण होता है तो ऊर्जा में कमी आती है और इस स्थिति में आबन्धन बनना संभव है। लेकिन कार्यशील आकर्षण बल एवं प्रतिकर्षण बल का परिणामी बल प्रतिकर्षण है तो ऊर्जा में वृद्धि होती है और आबन्धन बनना संभव नहीं होता है।
उदाहरण:
H2 अणु का बनना-जब दोनों H परमाणु एक-दूसरे से काफी दूरी पर स्थित हों तो उनके मध्य न तो कोई आकर्षण बल होता है और न ही कोई प्रतिकर्षण बल होता है। लेकिन जब दोनों H परमाणु को एक-दूसरे के पास लाया जाता है तो निम्नलिखित दो । परिस्थितियाँ हो सकती हैं
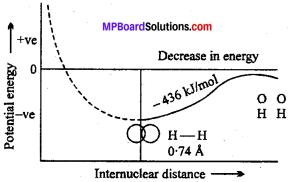
1. जब दो H परमाणु जिनके इलेक्ट्रॉन का चक्रण एक-दूसरे के समांतर है जब ये एक-दूसरे के निकट आते हैं तो स्थितिज ऊर्जा लगातार बढ़ती है क्योंकि दोनों इलेक्ट्रॉन -ve के मध्य प्रबल प्रतिकर्षण होता है। इसलिये यह आबन्धन अस्थिर होगा।
2. यदि विपरीत चक्रण वाले H परमाणु को पास-पास लाते हैं तो उनके बीच प्रबल आकर्षण बल होता है जिससे ऊर्जा में कमी आती है। विपरीत चक्रण के कारण दोनों नाभिकों के बीच इलेक्ट्रॉन घनत्व बढ़ जाता है जो दोनों नाभिकों को स्थिर वैद्युत आकर्षण बल द्वारा बांध लेता है, यह बंध सहसंयोजी बंध कहलाता है। इस न्यूनतम दूरी के पश्चात् यदि दोनों H परमाणुओं को और अधिक पास लाया जाता है तो नाभिक-नाभिक के मध्य प्रतिकर्षण बल बढ़ने लगता है जिससे ऊर्जा में लगातार वृद्धि होने लगती है और बंध पुनः अस्थिर होने लगता है।
प्रश्न 6.
दो अणुओं की संरचनाएँ दी गई हैं –
- इनमें से किस यौगिक में अंतर-अणुक हाइड्रोजन आबंध तथा अंतरा-अणुक हाइड्रोजन आबंध उपस्थित हैं?
- किसी यौगिक का गलनांक अन्य तथ्यों के अतिरिक्त, हाइड्रोजन आबंध पर भी निर्भर करता है। इसके आधार पर स्पष्ट कीजिए कि इन दोनों यौगिकों में से किसका गलनांक अधिक होगा?
- किसी यौगिक की जल में विलेयता, उसकी जल के साथ हाइड्रोजन आबंध बनाने की क्षमता पर निर्भर है। इनमें से कौन-सा यौगिक जल के साथ हाइड्रोजन आबंध सुगमतापूर्वक बनाकर इसमें अधिक विलेय रहेगा?
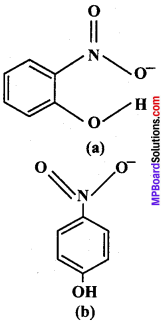
उत्तर:
1. यौगिक – (a) अंतरा-अणुक हाइड्रोजन आबंध बनायेगा। जब एक ही अणु में उपस्थित हाइड्रोजन परमाणु दो अधिक विद्युत्ऋणात्मक परमाणुओं (O, F, N आदि) के मध्य स्थित होता है तो अंतराअणुक हाइड्रोजन-आबंध बनाता है। ऑर्थो-नाइट्रोफिनॉल (यौगिक a) में, हाइड्रोजन परमाणु दो ऑक्सीजन परमाणुओं के मध्य स्थित होता है।
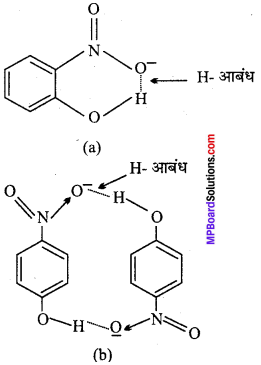
(b) यौगिक (b) अन्तर आण्विक हाइड्रोजन आबंध बनाता है। p – नाइट्रोफिनॉल (ii) में, – NO2 तथा – OH समूह के मध्य रिक्त स्थान है। अतः एक अणु के हाइड्रोजन परमाणु तथा दूसरे अणु के ऑक्सीजन परमाणु के मध्य अंतर-अणुक हाइड्रोजन आबंध बनाता है।
2. यौगिक (b) का गलनांक उच्च होगा क्योंकि इसके अनेक अणु परस्पर H – आबंध द्वारा जुड़ते हैं।
3. अंतरा-आण्विक H – आबंध के कारण, यौगिक (a) जल के साथ, H – आबंध नहीं बना पाता है जिसके कारण यह जल में कम विलेय है। जबकि यौगिक (b) के अणु जल के साथ सरलता से H – आबंध बना लेते हैं। जिसके कारण यह जल में विलेय है।
प्रश्न 7.
VSEPR सिद्धांत के आधार पर निम्न अणुओं की आकृति स्पष्ट कीजिए –
- CH4
- NH3
- H2O
उत्तर:
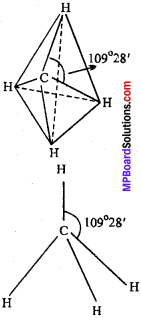
1. CH4 की आकृति:
मेथेन में केन्द्रीय परमाणु C, sp3 संकरित अवस्था में होता है तथा मेथेन का केन्द्रीय C परमाणु चार इलेक्ट्रॉन युग्म से घिरा रहता है तथा इसमें चार समान C – H बंध होते हैं। इसलिये अणु सममित तथा समचतुष्फलकीय होता है तथा C – Hबंधों में परस्पर प्रतिकर्षण बल न्यूनतम लगने के लिये ये चार बंध चतुष्फलकीय रूप में व्यवस्थित हो जाते हैं। यहाँ बंध कोण 109°28′ होता है।
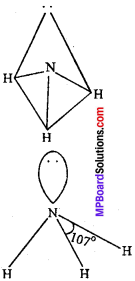
2. NH3 की आकृति:
अमोनिया में केन्द्रीय परमाणु N, sp3 संकरित अवस्था में होता है तथा यह चार इलेक्ट्रॉन जोड़ों से घिरा रहता है। इसलिये अणु की ज्यामिति सममित चतुष्फलकीय होनी चाहिये। लेकिन यहाँ केन्द्रीय परमाणु तीन इलेक्ट्रॉन युग्म तथा एक एकाकी इलेक्ट्रॉन युग्म से घिरा रहता है। इसलिये Lone pair – Bond pair में प्रतिकर्षण अधिक होता है जिसके कारण NH3 की संरचना त्रिकोणीय पिरामिडीय होती है और बंध कोण का मान 109°28′ से कम होकर 107° होता है।
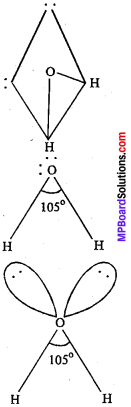
3. H2O की आकृति:
जल में केन्द्रीय परमाणु O, sp3 संकरित अवस्था में होता है तथा संकरित कक्षकों में से दो संकरित कक्षकों में युग्मित इलेक्ट्रॉन तथा अन्य दो संकरित कक्षकों में अयुग्मित इलेक्ट्रॉन होते हैं। ये अर्धपूर्ण संकरित कक्षक 2 हाइड्रोजन परमाणु के साथ अतिव्यापन कर H2O का निर्माण करते हैं। इसलिये H2O अणु की ज्यामिति spसंकरण के कारण चतुष्फलकीय होनी चाहिये तथा बंध कोण का मान 109°28′ होना चाहिये। यहाँ पर O दो बंधी इलेक्ट्रॉन युग्म तथा दो एकाकी इलेक्ट्रॉन युग्म द्वारा घिरा रहता है। इस एकाकी इलेक्ट्रॉन युग्म की उपस्थिति से अणु की ज्यामिति में विकृति उत्पन्न हो जाती है। इसलिये H2O की संरचना सममित चतुष्फलकीय न होकर – आकृति की होती है तथा बंध कोण का मान 109°28′ से घटकर 105° हो जाता है।
प्रश्न 8.
निम्नलिखित के कारण स्पष्ट कीजिए –
- सहसंयोजी आबंध दिशात्मक होते हैं जबकि आयनिक आबंध अदिशात्मक होते हैं।
- जल के अणु की रचना कोणीय होती है जबकि कार्बन-डाइऑक्साइड का अणु रेखीय होता है।
- एथाइन अणु रेखिक होता है।
उत्तर:
1. सहसंयोजी आबंध, आण्विक कक्षकों के अतिव्यापन द्वारा बनता है। अतिव्यापन की दिशा, आबंध की दिशा बताती है। आयनिक यौगिकों में, आयन का स्थिर वैद्युत क्षेत्र अदिशात्मक होता है। प्रत्येक धनायन ऋणायन के आकार के आधार पर, इनके किसी भी दिशा में घिरा हुआ होता है। इसी प्रकार ऋणायन, धनायनों से घिरे हुए होते हैं। यही कारण है कि सहसंयोजी आबंध दिशात्मक तथा आयनिक आबंध अदिशात्मक होते हैं।
2. H2O में, ऑक्सीजन दो एकाकी युग्मों के साथ sp3 संकरित होता है। sp3 संकरित कक्षक चतुष्फलक के चार शीर्षों की ओर सम्मुख रहते हैं। इनमें दो शीर्ष, हाइड्रोजन परमाणुओं द्वारा घेरे जाते हैं जबकि शेष दो शीर्ष, एकाकी युग्मों द्वारा घेरे जाते हैं। अतः एकाकी युग्म – एकाकी युग्म प्रतिकर्षण बल के कारण आबंध कोण 109.5° से घटकर 104.5° हो जाता है – जिसके कारण अणु ज्यामिति V – आकार अथवा मुड़ी हुई हो जाती है (कोणीय रचना)।
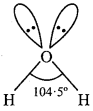
CO2 अणु में, कार्बन परमाणु sp- संकरित होता है। दो sp- संकरित कक्षक एक-दूसरे से विपरीत दिशाओं में 108° कोण बनाते हुए स्थित होते हैं।
![]()
यही कारण है कि H2O अणु की रचना कोणीय जबकि CO2 की रचना रैखिक होती है।
3. एथाइन में, दोनों कार्बन परमाणु sp- संकरित होते हैं तथा इनके दो (2px तथा 2py) कक्षक असंकरित होते हैं । ये दो sp- संकरित कक्षक एक-दूसरे से विपरित दिशाओं में 180° का कोण बनाते हुए स्थित होते हैं जिसके कारण एथाइन की रचना रैखिक होती है।
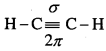
प्रश्न 9.
संयोजकता बंध सिद्धांत की प्रमुख अवधारणायें लिखिए एवं इस सिद्धांत की सीमायें बताइये।
उत्तर:
संयोजकता बंध सिद्धांत का प्रतिपादन हिटलर और लंदन ने किया था जिसे पॉलिग एवं स्लेटर ने आधुनिक स्वरूप प्रदान किया। इस सिद्धांत की प्रमुख अवधारणायें इस प्रकार हैं –
- इस सिद्धांत के अनुसार परमाणुओं के मध्य सहसंयोजक बंध उनके संयोजी कोश के अर्धपूरित परमाणु कक्षकों के आंशिक अतिव्यापन से बनते हैं।
- अतिव्यापन में भाग लेने वाले परमाणु कक्षकों में विपरीत चक्रण वाले इलेक्ट्रॉन स्थित होते हैं।
- बंध की प्रबलता अतिव्यापन की सीमा पर निर्भर होती है। अधिक अतिव्यापन होने पर प्रबल बंध बनता है।
- समान स्थायित्व, समान ऊर्जा तथा समान सममिति वाले दो कक्षकों के मध्य अधिक दिशात्मक दृढ़ बंध बनता है।
- अतिव्यापन तथा इलेक्ट्रॉन के युग्मन के फलस्वरूप ऊर्जा मुक्त होती है तथा निकाय निम्न ऊर्जा अवस्था को प्राप्त कर लेता है।
- दोनों में से प्रत्येक कक्षक का पूर्ण बंध कक्षक प्राप्त होता है और इस प्रकार उसे दोनों परमाण्वीय नाभिकों की संपत्ति माना जाता है।
संयोजकता बंध सिद्धांत की सीमायें:
- इस सिद्धांत के अनुसार O2 के अणु में कोई अयुग्मित इलेक्ट्रॉन नहीं हैं। अतः ऑक्सीजन की प्रकृति प्रतिचुम्बकीय होनी चाहिए परन्तु वास्तव में O, अणु अनुचुम्बकीय होता है।
- उपसहसंयोजक बंध के निर्माण के विषय में कोई व्याख्या नहीं करता है।
- H2 जैसे आयनों के निर्माण की व्याख्या करने में यह सिद्धांत असफल है।
- यह अनुनाद के विषय में कोई जानकारी देने में असमर्थ है।
प्रश्न 10.
आबंध कोटि किसे कहते हैं? आबंध कोटि से प्राप्त होने वाली जानकारियाँ लिखिए।
उत्तर:
आबंध कोटि-बंधी आणविक कक्षक में इलेक्ट्रॉन की संख्या तथा प्रतिबंधी आण्विक कक्षक में इलेक्ट्रॉन की संख्या के अंतर के आधे को आबंध कोटि कहते हैं।

जानकारी:
- यदि आबंध कोटि का मान धनात्मक हो तो अणु स्थायी होता है और यदि आबंध कोटि का मान ऋणात्मक या शून्य है तो अणु अस्थायी होता है।
- आबंध कोटि अणु में उपस्थित सहसंयोजी बंधों की संख्या के बराबर होती है।
- यदि आण्विक कक्षक में उपस्थित इलेक्ट्रॉन युग्मित है तो अणु प्रति चुम्बकीय होता है और यदि आण्विक कक्षक में उपस्थित इलेक्ट्रॉन अयुग्मित है तो अणु अनुचुम्बकीय होता है।
- आबंध कोटि बंध वियोजन ऊर्जा के समानुपाती होती है।
- आबंध कोटि बंध लम्बाई के व्युत्क्रमानुपाती होती है।
प्रश्न 11.
आण्विक ऊर्जा स्तर के आधार पर N,अणु के आरेख चित्र द्वारा प्रदर्शित कीजिए।
उत्तर:
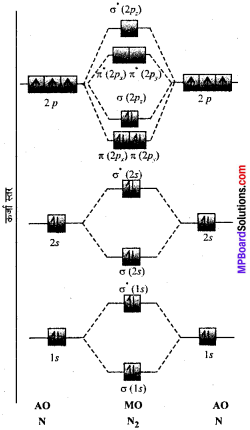
N2अणु:
एक नाइट्रोजन परमाणु में 7 इलेक्ट्रॉन होते हैं। 1s2,2s22p3 अत: N2 अणु में 14 इलेक्ट्रॉन होगें और उसका आण्विक कक्षक आरेख दर्शाये अनुसार होगा।
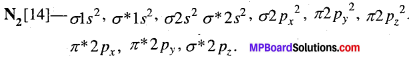
नाइट्रोजन अणु का बन्धक्रम निम्न प्रकार से ज्ञात किया जा सकता है –
बन्धी इलेक्ट्रॉन की संख्या = 10
विपरीत बन्धी इलेक्ट्रॉन की संख्या = 10
अत: बन्धक्रम = \(\frac{1}{2}\)(Nb – Na) = (10 – 4) = 3
प्रश्न 12.
आण्विक कक्षक ऊर्जा स्तर आरेख का प्रयोग करते हुए दर्शाइए कि निऑन का द्विपरमाणुक अणु की प्रकृति में अस्तित्व नहीं है।
उत्तर:
10Ne का इलेक्ट्रॉनिक विन्यास – 10Ne = 1s2, 2s2, 2px2 2py2 2pz2
आण्विक कक्षक ऊर्जा स्तर आरेख –
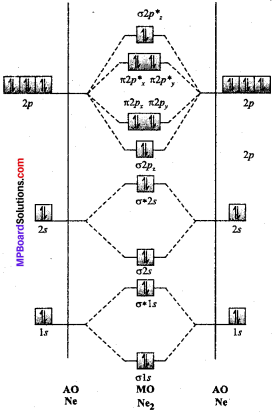
आबंध कोटि = \(\frac{1}{2}\)(Nb – Na) = \(\frac{1}{2}\) (10 – 10) = 0
आबंध कोटि शून्य का अर्थ है कि दो Ne परमाणुओं के मध्य कोई आबंध नहीं बनता है। अतः Ne2 (द्विपरमाणुक अणु) का प्रकृति में कोई अस्तित्व नहीं होता है।
प्रश्न 13.
O2 अणु के लिए आण्विक कक्षक आरेख बनाइये।
उत्तर:
ऑक्सीजन अणु-एक ऑक्सीजन परमाणु में 8 इलेक्ट्रॉन होते हैं –
1s2, 2s2 2p4 अत: O2 अणु में 16 इलेक्ट्रॉन होंगे और उसका आण्विक कक्षक आरेख दर्शाये अनुसार होगा।
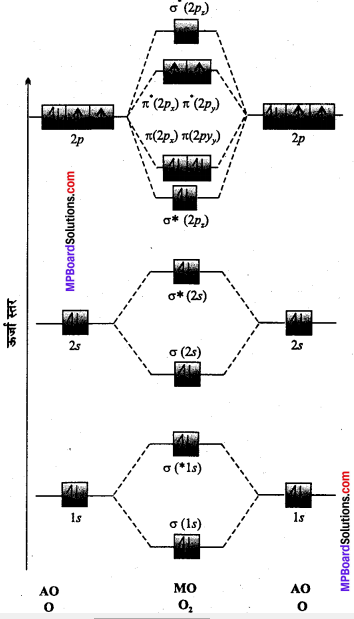
बन्ध क्रम = \(\frac{1}{2}\)[Nb – Na] = \(\frac{1}{2}\)[10 – 6] =2
ऑक्सीजन अणु के आण्विक कक्षकों में दो अयुग्मित इलेक्ट्रॉन होने से अणु अनुचुम्बकीय (Paramagnetic) होता है।